时间:2019-06-25 22:35:07
1、填空题 有pH=1的盐酸、硫酸、醋酸三瓶溶液(用>、<、=填空,下同).
(1)设三种溶液的物质的量浓度依次为C1、C2、C3,则其关系是______.
(2)取相同体积的三种酸分别加入蒸馏水稀释到pH=3,需水的体积依次为V1、V2、V3,则其关系是______.
(3)完全中和体积和物质的量浓度均相同的Ba(OH)2溶液时,需三种酸的物质的量依次为n1、n2、n3,则其关系是______.
(4)取同体积的酸的溶液分别加入足量的锌粉,反应开始放出H2的速率依次为υ1、υ2、υ3,则其关系是______.
2、选择题 下列物质中,属于强电解质的是
A.CO2
B.盐酸
C.BaSO4
D.NaOH溶液
3、选择题 依据右图分析,下列叙述不正确的是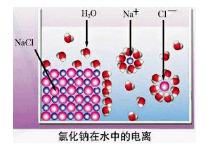
A.氯化钠是由钠离子和氯离子构成的
B.氯化钠的电离方程式为:NaCl =Na+ + Cl―
C.氯化钠的电离过程需要通电才能完成
D.氯化钠在水中形成能自由移动的水合钠离子和水合氯离子
4、填空题 草酸(H2C2O4)是二元弱酸,25℃时,H2C2O4:K1=5.4×10-2,K2=5.4×10-5;H2CO3:K1=4.5×10-7,K2=4.7×10-11。
(1)KHC2O4溶液呈__________性(填“酸”、“中”或“碱”)。
(2)下列化学方程式可能正确的是?。
A.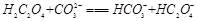
B.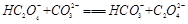
C.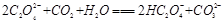
D.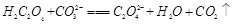
(3)常温下,向10 mL 0.01 mol・L-1H2C2O4溶液中滴加0.01 mol・L-1的KOH溶液V mL,回答下列问题:
①当V<10时,反应的离子方程式为______________________________________________。
②若溶液中离子浓度有如下关系:c(K+)=2c(C2O42-)+c(HC2O4-),则pH______7(填“>”“<”或“=”),V________10(填“>”“<”或“=”)。
③当溶液中离子浓度有如下关系:c(K+)=c(C2O42-)+c(HC2O4-)+c(H2C2O4),则溶液中溶质为____________,V________10(填“>”、“<”或“=”)。
④当V=20时,溶液中HC2O4-、C2O42-、H2C2O4、OH-的物质的量浓度从大到小的顺序为____________________________________________________________________________________。
5、选择题 在甲酸的下列性质中,可以证明它是弱电解质的是( )
A.1mol/L甲酸溶液中c(H+)约为1×10-2mol/L
B.甲酸能与水以任意比互溶
C.10mL 1mol/L甲酸恰好跟10 mL 1mol/L NaOH溶液完全反应
D.甲酸的导电性比强酸溶液的导电性弱。