时间:2017-07-18 02:34:05
1、选择题 共价键的断裂有均裂和异裂两种方式,即均裂: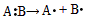 ,异裂:
,异裂: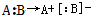 。下列化学反应中发生共价键均裂的是
。下列化学反应中发生共价键均裂的是
[? ]
A. 2K+2H2O=2KOH+H2↑
B. 2Na+2C2H5OH→2C2H5ONa+H2↑
C.?Na2CO3+ H2O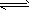 NaHCO3 + NaOH
NaHCO3 + NaOH
D. CH3COOH +C2H5OH H2O+CH3COOC2H5
H2O+CH3COOC2H5
2、选择题 经X射线研究证明:PCl5在固体状态时,由空间构型分别为正四面体和正八面体两种离子构成。下列关于PCl5的推断正确的是(?)
A? PCl5固体是分子晶体
B? PCl5固体有良好的导电性
C? PCl5晶体由[PCl4]+和[PCl6]-构成,其离子数目之比为1∶1
D? PCl5晶体由[PCl3]2+和[PCl7]2-构成,其离子数目之比为1∶1
3、填空题 (14分)下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。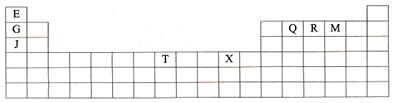
(1)T3+的核外电子排布式是:?
(2)Q、R、M的第一电离能由大到小的顺序是?(用元素符号表示)
(3)根据下列说法填空:
①G单质的熔点高于J单质,是因为?
②将J2M2溶于水,要破坏?(离子键、极性共价键、非极性共价键)
③RE3沸点高于QE4,是因为?
④一个Q2E4分子中E的?轨道与Q的?轨道形成σ键。
(4)G与R单质直接化合生成一种离子化合物G3R。该晶体具有类似石墨的层状结构。每层中,G原子构成平面六边形,每个六边形的中心有一个R原子。层与层之间还夹杂一定数量的原子。请问这些夹杂的原子应该是 ??(填G或R的元素符号)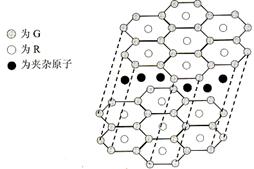
4、选择题 下列的晶体中,化学键种类相同,晶体类型也相同的是?
[? ]
A.SO2与SiO2?
B.CO2与H2O?
C.NaCl与HCl?
D.CCl4与KCl
5、简答题 已知四种短周期元素W、X、Y、Z的原子序数依次增大,请结合表中信息回答下列问题:
W
X
Y
Z
结构或性质
最高价氧化物对应的水化物与其气态氢化物反应得到离子化合物
焰色反应呈黄色
在同周期主族元素形成的简单离子中,离子半径最小
最高正化合价与最低负化合价之和为零
(1)Z在元素周期表中位于______族.
(2)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他三种物质发生化学反应,该元素是______(填元素符号).
(3)①下列可作为比较X和Y金属性强弱的依据是______(填序号).
a.自然界中的含量
b.相应氯化物水溶液的pH
c.单质与水反应的难易程度
d.单质与酸反应时失去的电子数
②从原子结构的角度解释X的金属性强于Y的原因:______,原子半径X>Y,所以原子核对最外层电子的吸引力X<Y,失电子能力X>Y.
(4)W的一种氢化物HW3可用于有机合成,其酸性与醋酸的相当.体积和浓度均相等的HW3与X的最高价氧化物对应的水化物混合,反应的化学方程式是______,混合后溶液中离子的浓度由大到小的顺序是______.