时间:2017-07-18 02:34:05
1、填空题 A、B、C、D、E、F、G七种短周期主族元素的原子序数依次增大,D、G同主族,A与B、C、D能形成电子数相同的二种常见分子,E、F的原子序数之和是D的原子序数的3倍,D、E、F的简单离子具有相同电子层结构.
(1)三种元素的名称.B______,D______,F______.
(2)A与D、A与G均可形成18e-的化合物.两种化合物在水溶液中反应的化学方程式为:______
(3)A、D、E三种元素中的两种或三种形成的物质中,含有非极性键的离子化合物的电子式为:______;只含离子键的化合物的电子式为:______.
(4)E离子的半径______(填“大于”“小于”或“等于”)?F离子的半径;E?和F元素最高价氧化物对应的水化物之间反应的离子方程式为:______.
(5)写出由上述各种元素形成的粒子中与BC-电子数相等的三种分子的化学式______、______、______.
参考答案:由短周期主族元素的原子序数依次增大,A与B、C、D能形成电子数相同的二种常见分子,由常见的10e-和18e-微粒可知,则A为氢,B为碳、C为氮、D为氧;D、G同主族,则G为硫;E、F的原子序数之和是D的原子序数的3倍,D、E、F的简单离子具有相同电子层结构,由8×32=12可知,E为钠,F为铝,
(1)B为碳,D为氧,F为铝,故答案为:碳;氧;铝;
(2)A与D、A与G均可形成18e-的化合物为H2O2、H2S,H2O2具有氧化性,H2S具有还原性,二者发生氧化还原反应为H2O2+H2S=S↓+2H2O,
故答案为:H2O2+H2S=S↓+2H2O;
(3)A、D、E三种元素中的两种或三种形成的物质有Na2O2、Na2O、NaOH等,含有非极性键的离子化合物为Na2O2,其电子式为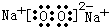
,只含离子键的化合物为Na2O,其电子式为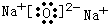
,故答案为: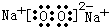
;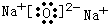
;
(4)E、F的简单离子具有相同电子层结构,原子序数大的离子半径小,则铝离子的半径小,E?和F元素最高价氧化物对应的水化物分别为NaOH、Al(OH)3,发生的离子反应为
Al(OH)3+OH-=AlO2-+2H2O,故答案为:大于;Al(OH)3+OH-=AlO2-+2H2O;
(5)BC-电子数为6+7+1=14,N2的电子数为7×2=14,CO的电子数为6+8=14,C2H2的电子数为6×2+1×2=14,故答案为:N2;CO;C2H2.
本题解析:
本题难度:一般
2、选择题 在短周期中的X和Y两种元素可组成化合物XY3,则下列说法中正确的是(? )
A.若X的原子序数是m,则Y的原子序数必定是m 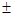 4
4
B.XY3晶体一定属于离子晶体
C.X与Y可属于两个不同周期,也可属于同一周期
D.X的原子半径小于Y的原子半径
参考答案:C
本题解析:组成化合物XY3有AlCl3 NH3 PH3 SO3 BF3
A、比如氨气它的原子序数就不符合m 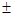 4,故错
4,故错
B、氨气属于分子晶体,故错
D、当为氯化铝的时候,铝的半径大于氯的。故错
点评:本题考查学生对元素周期表和元素周期律知识的掌握,利用举例法能快速准确的解题
本题难度:简单
3、选择题 近期《美国化学会志》报道,中国科学家以二氧化碳为碳源,金属钠为还原剂,在470℃、
80MPa条件下合成出金刚石,具有深远意义。下列说法不正确的是
[? ]
A.由二氧化碳合成金刚石是化学变化
B.金刚石是碳的一种同位素
C.钠被氧化最终生成碳酸钠
D.金刚石中只含有非极性共价键
参考答案:B
本题解析:
本题难度:简单
4、选择题 氢键既可以存在于分子之间,也可以存在于分子内部的原子团之间,如邻羟基苯甲醛分子( ) 内的羟基与醛基之间即存在氢键(分子内氢键),对羟基苯甲醛分子( HO
) 内的羟基与醛基之间即存在氢键(分子内氢键),对羟基苯甲醛分子( HO CHO )之间存在氢键(分子间氢键)。则两者的熔点、沸点的相对大小关系是(?)
CHO )之间存在氢键(分子间氢键)。则两者的熔点、沸点的相对大小关系是(?)
A.前者>后者
B.前者<后者
C.前者=后者
D.无法估计
参考答案:B
本题解析:由于分子间氢键强于分子内的氢键,所以邻羟基苯甲醛的熔沸点小于对羟基苯甲醛熔沸点,答案选B。
点评:该题是常识性知识的考查,试题基础性强,紧扣教材基础知识,意在调动学生的学习兴趣和学习积极性,提高学生灵活运用基础知识解决实际问题的能力。
本题难度:一般
5、填空题 在HF、H2O、NH3、CS2、CH4、N2分子中:
(1)以非极性键结合的非极性分子是______________。
(2)以极性键结合,具有直线形结构的非极性分子是___________。
(3)以极性键结合,具有三角锥形结构的极性分子是___________。
(4)以极性键相结合,具有正四面体结构的非极性分子是____________。
(5)以极性键相结合,具有V形结构的极性分子是_____________。
(6)以极性键相结合,而且分子极性最大的是____________。
参考答案:(1)N2
(2)CS2
(3)NH3
(4)CH4
(5)H2O
(6)HF
本题解析:
本题难度:一般