1
4
P4O10(s)△H2=-738.5kJ/mol,则白磷转化为红磷的热化学方程式______.相同的状况下,能量较低的是______;白磷的稳定性比红磷______(填“高”或“低”).
2、选择题 1mol白磷转化为红磷时放出18.39kJ热量,已知:P4(白磷,s)+5O2(g)═2P2O5(s)△H=-a?kJ/mol(a>0);4P(红磷,s)+5O2(g)═2P2O5(s)△H=-b kJ/mol(b>0),则a和b的关系是( )
A.a>b
B.a=b
C.a<b
D.无法确定
3、简答题 碳酸锶广泛应用于电子工业.以天青石(主要成分为SrSO4)为基本原料制备碳酸锶.
(1)碳还原法制备.
①已知:SrSO4(s)+4C(s) 高温
4CO(g)+SrS(s);△H=+akJ-mol-1
SrSO4(s)+2C(s)高温
2CO2(g)+SrS(s);△H=+bkJ-mol-1
则反应C(s)+CO2(g)高温
2CO(g)的△H=______kJ-mol-1.
②SrS是强碱弱酸盐,热水中发生水解的化学反应方程式为______.
③水解所得Sr(OH)2与NH4HCO3按照物质的量比1:1投料制备SrCO3,则化学反应方程式为______.
(2)湿法制备.(已知:Ksp(SrSO4)=3.2×10-7,Ksp(SrCO3)=1.1×10-10)
①将天青石矿粉与Na2CO3溶液搅拌混匀、加热,发生的离子反应方程式为______.
②当转化完成时,混合液中c(CO
2-3
)=1.0×10-3mol/L,c(SO
2-4
)=______mol/L.
4、选择题 CH4与Cl2反应的历程有:
①Cl-Cl→2Cl· ΔH= 243 kJ·mol-1
②Cl·+CH3-H → ·CH3+H-Cl ΔH= 4 kJ·mol-1
③·CH3+Cl-Cl → CH3-Cl +Cl· ΔH= -106 kJ·mol-1
则反应CH4(g)+Cl2(g) =CH3Cl(g)+HCl(g)的焓变应为 [???? ]
A.110kJ·mol-1
B.141 kJ·mol-1
C.-102 kJ·mol-1
D.102kJ·mol-1
5、选择题 已知:①C?(s)+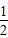 O2(g)CO?(g)△H=-110.5kJ?mol?-1 O2(g)CO?(g)△H=-110.5kJ?mol?-1
②C?(s)+O2?(g)CO2?(g)△H=-393.51kJ?mol?-1
则反应:C?(s)+CO2(g)2CO?(g)?的△H为( ? ) A.-283.01?kJ?mol?-1
B.+504.00?kJ?mol?-1
C.+283.01?kJ?mol?-1
D.+172.51?kJ?mol?-1
微信搜索关注"91考试网"公众号,领30元,获取公务员事业编教师考试资料40G
|