1������� �о�NOx��SO2��CO�ȴ�����Ⱦ����Ĵ�������������Ҫ���塣
��1��������CO��SO2�̵�����Ⱦ��һ�ַ����ǽ����ڴ���������ת��Ϊ����S��
��֪��
��CO��g��+?1/2O2(g)��CO2��g��???��H=��283.0kJ/mol???
��S��s��+?O2(g)��SO2��g��?????��H=��296.0kJ/mol?
�˷�Ӧ���Ȼ�ѧ����ʽ��___________________��
��2��������������ɹ⻯ѧ�����ͳ�������ĵ���Ҫ���塣
��֪�� ?????
��?CO��g��+NO2(g)��NO(g)+CO2(g)???��H=��akJ/mol?(a��0) ?????
��?2CO��g��+2NO(g)��N2(g)+2CO2(g)???��H=��bkJ/mol?(b��0)
���ñ�״����?3.36LCO��ԭNO2��N2��CO��ȫ��Ӧ��������������ת�Ƶ��ӵ����ʵ���Ϊ_______mol���ų�������Ϊ________kJ���ú���a��b�Ĵ���ʽ��ʾ����
��3����CH4����ԭNOxҲ�������������������Ⱦ�����磺 ?????
��CH4��g��+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)????��H1����574kJ/mol?�� ?????
��CH4��g��+4NO?(g)=2N2(g)+CO2(g)+2H2O(g)????��H2������
��1molCH4��ԭNO2��N2���������зų�������Ϊ867KJ�����H2=_________��
2��ѡ���� ��֪��(1)
��2��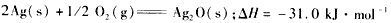
��Zn(s) +Ag 2O(s)=ZnO(s) +2Ag(s)�ġ�H���� [???? ]
A��-317.3 kJ/mol
B��-379.3 kJ/mol
C��-332. 8 kJ/mol
D��317.3 kJ/mol
3������� ��֪�����Ȼ�ѧ����ʽ��
(1)Fe2O3(s)+3CO(g)====2Fe(s)+3CO2(g) ��H=��25kJ��mol-1
(2)3Fe2O3��s��+CO(g)====2Fe3O4(s)+CO2(g) ��H=��47kJ��mol-1
(3)Fe3O4(s)+CO(g) ====3FeO(s)+CO2(g) ��H= +19 kJ��mol-1
д��FeO(s)��CO��ԭ��Fe��CO2���Ȼ�ѧ����ʽ��_________________________________��
4������� ������Ⱦ������������ȫ���������ŵĿ��⣮
��1��Ϊ�˼��ٿ�����SO2���ŷţ�����ȡ�Ĵ�ʩ�У�
�ٽ�úת��Ϊ�������ȼ�ϣ���֪��H2��g��+
1
2
O2��g���TH2O��g����H1=-241.8kJ?mol-1��
C��s��+1
2
O2��g���TCO��g����H2=-110.5kJ?mol-1��̿��ˮ������Ӧ����CO���Ȼ�ѧ����ʽΪ______��
��ϴ�Ӻ�SO2���������������ʿ���ϴ�Ӽ�����______������ţ���
a��Ca��OH��2b��CaCl2 c��Na2CO3d��NaHSO3
��2��CO�ڴ��������¿�����H2��Ӧ���ɼ״���CO��g��+2H2��g��?CH3OH��g�������ܱ������г���10molCO��20molH2��CO��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ1��ʾ��
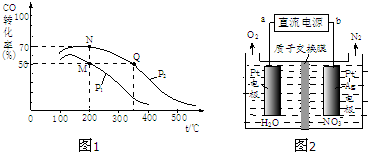
��M��N����ƽ��״̬�£������������ʵ����ʵ���֮��Ϊ��n��M���ܣ�n��N����=______��
����M��N��Q�����ƽ�ⳣ��KM��KN��KQ�Ĵ�С��ϵΪ______��
��3�����������͵绯ѧ���ⷨ����������ˮ�������ε���Ⱦ��
�ٴ��������У���H2��NO3-��ԭΪN2��һ��ʱ�����Һ�ļ���������ǿ����÷�Ӧ���ӷ���ʽΪ______��
�ڵ绯ѧ����NO3-��ԭ����ͼ2��ʾ����Դ����Ϊ______���a����b���������ܷ�ӦΪ4NO3-+4H+ͨ��
.
5O2��+2N2��+2H2O����������ӦʽΪ______��
5������� �Ȼ�ѧ����ʽ�е�Hʵ����������ѧ�е�һ���������������ʡ�һ����ϵ���ʣ�H���ľ���ֵ��ĿǰΪֹ��û�а취��ã�������ϵ�����仯ʱ�����ǿ��Բ����ϵ���ʵı仯�����ʱ䣬�á���H����ʾ����H��H����̬����H��ʼ̬����
��1����ѧ��Ӧ�еĦ�H����_______?����ʽ���ֵġ����ڻ�ѧ��ӦA+B=C+D����H��A����H(B)��H��C��+H(D)����÷�Ӧ�Ħ�HΪ____0������ڡ�����С�ڡ������÷�Ӧ��?_____������ȡ������ȡ�����Ӧ��?
��2����һ���о���������ѧ��Ӧ���ʱ��뷴Ӧ���������ļ����йء�?
��֪��298Kʱ��
H2(g)+Cl2(g)=2HCl(g)??��H=?-185?kJ/mol?��H��H2��=?436?kJ/mol, ��H��Cl2��=?247?kJ/mol��??��H��HCl��=?________________��
��3��Hess?G��H���ܽ����ʵ����ʵ֮����Ϊ��ֻҪ��ѧ��Ӧ��ʼ̬����̬ȷ������ѧ��Ӧ�Ħ�H���Ƕ�ֵ���뷴Ӧ��;���ء�����������ġ�Hess���ɡ���
��֪��
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)????��H?=?-25?kJ/mol???????
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)???��H?=?-47?kJ/mol????
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)??????��H?=?+19?kJ/mol
��д��CO��ԭFeO���Ȼ�ѧ����ʽ_______________________��?
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա��ҵ���ʦ��������40G
|
|
|