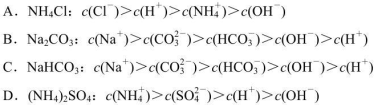时间:2017-08-22 14:34:55
1、选择题 下列溶液,阴离子总浓度最大的是( )
A.0.2 mol / L NaCl
B.0.1 mol / L Ba(OH)2
C.0.2 mol / L K2S
D.0.2 mol / L (NH4)2SO4
2、简答题 某二元酸H2A的电离情况为:H2A=H++HA-;HA-?H++A2-.请据此回答下列有关问题:
(1)Na2A溶液呈______(填“弱酸性”、“中性”或“弱碱性”),其理由是______(用离子方程式表示).
(2)写出NaHA溶液中溶质电离常数(Ka)的表达式______.
(3)如果25℃时,0.10mol?L-1?H2A溶液的pH=-lg0.11,则0.10mol?L-1的H2A溶液中c(A2-)=______mol?L-1.
3、选择题 部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
4、选择题 下列溶液中微粒的物质的量浓度关系正确的是
A.25℃时,pH=7的NH4Cl与NH3・H2O混合溶液:c(H+)= c(OH-)= c(NH )=c(Cl-)
)=c(Cl-)
B.0.1mol/LNa2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S)
C.25℃时,pH=2的HCOOH与pH=12的NaOH等体积混合:c (HCOO-)+ c(H+)>c(Na+)+c(OH-)
D.0.1mol/LNa2CO3溶液与0.1mol/L NaHCO3溶液等体积混合:2c(CO32-)+2c(HCO3-)+2c(H2CO3)=3c(Na+)
5、选择题 由下列物质所配成的0.l mol  的溶液中,离子浓度由大到小的顺序正确的是
的溶液中,离子浓度由大到小的顺序正确的是