时间:2017-08-09 23:43:30
1、实验题 某探究小组用KMnO4酸性溶液与H2C2O4溶液反应过程中溶液紫色消失的方法,研究影响反应速率的因素。该反应的离子方程式为:2MnO4-+5H2C2O4+ 6H+=2Mn2+ + 10CO2↑+ 8H2O 该实验条件作如下限定:
①所用KMnO4酸性溶液的浓度可选择:0.01 mol·L-1、0.001 mol·L-1;
②所用H2C2O4溶液的浓度可选择:0.1 mol·L-1、0.2 mol·L-1;
③催化剂的用量可选择0g、0.5g;
④实验温度可选择298K、323K。
(1)每次实验KMnO4酸性溶液的用量均为4 mL、H2C2O4溶液的用量均为2mL。如果要探究反应物浓度、温度、催化剂对反应速率的影响,通过变换这些实验条件,至少需要完成____________个实验进行对比即可得出结论。
(2)在其它条件相同的情况下,某同学改变KMnO4酸性溶液的浓度,测得以下实验数据:(从混合振荡均匀开始计时)? 
①用0.001 mol·L-1 KMnO4酸性溶液进行实验时KMnO4的平均反应速率_________(忽略混合前后溶液的体积变化)
②若不经过计算,直接看表中的褪色时间长短来判断浓度大小与反应速率的关系是否可行?_________(填“是”或“否”) 。若不可行(若认为可行则不填),请设计可以通过直接观察褪色时间长短来判断的改进方案:_________________ 。
参考答案:(1)4
(2)① 1×10-4 mol·L-1·min-1
② 否; 取过量的体积相同、浓度不同的草酸溶液分别同时与体积相同、浓度相同的高锰酸钾酸性溶液反应。
本题解析:
本题难度:一般
2、实验题 (10分) 无水CuSO4在强热下会发生分解反应:
CuSO4 CuO + SO3↑
CuO + SO3↑
2SO3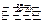 2
2 SO2↑+ O2↑
SO2↑+ O2↑
某研究性学习小组设计了下图所示装置(夹持仪器已略去),利用D管在反应前后的质量差计算分解的无水CuSO4的质量。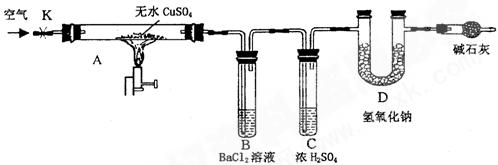
实验步骤:
①称量反应前D 管的质量。
管的质量。
②连接好装置,关闭K,加热硬质玻璃管A一定时间后,停止加热 。
。
③待硬质玻璃管A冷却后,打开K,通入一段时间的空气。
④再称量D管,得其反应前后的质量差为m。
(1)B管中出现的现象是__________________________________________________。
有关离子方程式是__________________________________________________
(2)B管的作用是除去混合气体中的SO3,实验过程中发现B管的温度明显升高,主要原因是______________________
(3)按上述方法实验,假设B、C、D对气体的吸收均完全,并忽略空气中CO2的影响,能否根据m计算分解的无水CuSO4的质量?___________
原因是__________________________________________________________。
参考答案:(1)有气泡冒出,产生白色沉淀,且明显放热(2分)
SO3 + H2O + Ba2+= BaSO4↓+ 2H+
或SO3 + H2O = 2H++SO42-, SO42- + Ba2+= BaSO4↓(4分)
(2) SO3溶于水放热(2分)
(3)不能(2分),SO3不能完全分解为SO2和O2, 且部分SO2会溶解在溶液中(4分)
本题解析:略
本题难度:简单
3、实验题 14、用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液时,下列实验操作会引起测定结果偏高的是:
①用天平称量NaOH固体时,将NaOH放在右盘,砝码放在左盘,并移动游码使之平衡。
②滴定前有气泡,滴定终点无气泡。
③用蒸馏水洗净锥形瓶后盛入待测NaOH溶液进行滴定。
④用蒸馏水洗净酸滴定管后盛入标准盐酸进行滴定。
⑤滴定终点读取酸滴定管数据时,仰视刻度线。
参考答案:B
本题解析:误差的分析的决定式是C碱=(C酸×V酸)/v碱
①物码倒置,相当于称量的氢氧化钠少了,浓度自然偏低 ②滴定前有气泡,滴定终点无气泡,相当于酸用多了,所以浓度偏大 ③相当于稀释了氢氧化钠,浓度偏低④相当于把标准酸稀释了,结果,用的酸的体积就会偏大,所以,浓度偏大⑤仰视,会把读书看大,所以偏大。故选B。
点评:掌握规律,只要记住,无论如何稀释,被滴定物质的总量不变,所以相应使用的滴定剂的量也不会变化。问题便很简单了。
本题难度:一般
4、简答题 两个学习小组用图装置探究乙二酸(HOOC-COOH)受热分解的部分产物.
(1)甲组:①按接口顺序:a-b-c-d-e-f-g-h连接装置进行实验.B中溶液变浑浊,证明分解产物有______;装置C的作用是______;E中溶液变浑浊,D中的现象是______,证明分解产物有______.
②乙二酸受热分解的化学方程式为______.
(2)乙组:
①将接口a与j连接进行实验,观察到F中生成的气体可使带火星的木条复燃,则F中最主要反应的化学方程式为______.
②从A-F中选用装置进行实验,证明甲组通入D的气体能否与Na2O2反应.最简单的装置接口连接顺序是______;实验后用F中的固体进行验证的方法是______(可另选试剂).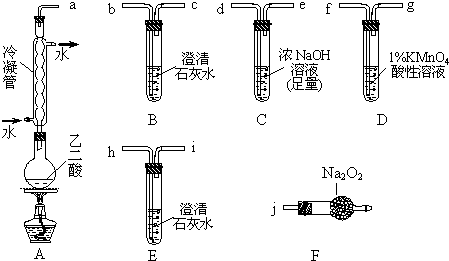
参考答案:(1)①B中澄清石灰水变浑浊,证明分解产物有CO2产生;装置C的作用是充分除去CO2,防止对后继实验产物检验的干扰;E中澄清石灰水变浑浊,说明有CO2产生,乙二酸产生的CO2在C装置中已经被NaOH吸收完全,CO2的产生来源于D装置中高锰酸钾对CO的氧化,D中现象为溶液褪色(或变浅),证明分解产物有CO,故答案为:CO2;充分除去CO2;溶液褪色或变浅;?CO;?
②乙二酸受热分解的化学方程式为:HOOC-COOH加热
本题解析:
本题难度:一般
5、选择题 配制一定体积、一定物质的量浓度的溶液,正确情况对实验结果产生偏低影响的是
A.容量瓶中原有少量蒸馏水
B.溶解所用的烧杯未洗涤
C.定容时仰视观察液面
D.定容时俯视观察液面
参考答案:B C
本题解析:A 容量瓶中原有少量蒸馏水,对配置结果无影响
B?溶解所用的烧杯未洗涤,说明溶质未全部转移到容量瓶中,所配溶液浓度偏低
C 定容时仰视观察液面,比平视时加得水多,所配溶液浓度偏低
D 定容时俯视观察液面,比平视时加得水少,所配溶液浓度偏高。
本题难度:一般