时间:2017-07-18 02:34:05
1、选择题 某有机物A由C、H、O三种元素组成,相对分子质量为90.将9.0g?A?完全燃烧的产物依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g.A能与NaHCO3溶液发生反应,且2分子A之间脱水可生成六元环化合物.有关A的说法正确的是( )
A.分子式是C3H8O3
B.A催化氧化的产物能发生银镜反应
C.0.1molA与足量Na反应产生2.24LH2(标准状况)
D.A在一定条件下发生缩聚反应的产物是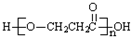
参考答案:C
本题解析:
本题难度:一般
2、填空题 已知元素X、Y、Z、W、Q均为短周期元素,原子序数依次增大,X基态原子的核外电子分布在3 个能级,且各能级电子数相等,Z是地壳中含量最多的元素,W是电负性最大的元素,元素Q的核电荷数等于Y、W原子的最外层电子数之和。另有R元素位于元素周期表第4周期第Ⅷ族,外围电子层有2个未成对电子,请回答下列问题。
(1)微粒XZ32-的中心原子杂化类型为?化合物YW3的空间构型为?。
(2)R基态原子的电子排布式为?,元素X、Y、Z的第一电离能由大到小的顺序为
?(用元素符号表示)。
(3)一种新型导体晶体的晶胞如右图所示,则该晶体的化学式为?,其中一个Q原子紧邻?个R原子。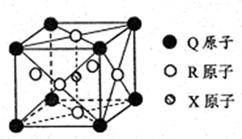
(4)R的氢氧化物能溶于含XY-离子的溶液生成一种配离子[R(XY)4]2-,该反应的离子方程式是?弱酸HXY分子中存在的σ键与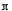 键的数目之比为?。
键的数目之比为?。
参考答案:(16分,每空2分)(1)sp2?三角锥形?(2)1s22s22p63s23p63d84s2或[Ar]3d84s2? N>O>C
(3)MgNi3C? 12?(4)Ni(OH)2+4CN-=[Ni(CN)4]2-+2OH-? 1:1
本题解析:X基态原子的核外电子分布在3 个能级,且各能级电子数相等,这说明X的原子序数是2+2+2=6,因此X是碳元素。Z是地壳中含量最多的元素,则Z是氧元素;Y的原子序数介于X与Z之间,所以Y是氮元素。W是电负性最大的元素,所以W是氟元素。元素Q的核电荷数等于Y、W原子的最外层电子数之和,因此Q的原子序数=5+7=12,则Q是镁元素。另有R元素位于元素周期表第4周期第Ⅷ族,外围电子层有2个未成对电子,所以R是镍元素。
(1)微粒XZ32-是CO32-,中心原子碳原子含有的孤对电子对数=(4+2-3×2)÷2=0,所以该微粒的空间构型是平面正三角形,则碳原子杂化类型为 sp2杂化;化合物YW3是NF3,根据价层电子对互斥理论可知,中心原子N原子含有的孤对电子对数=(5-3×1)÷2=1,因此NF3分子空间构型为三角锥形结构。
(2)根据构造原理可知,镍元素基态原子的电子排布式为1s22s22p63s23p63d84s2或[Ar]3d84s2;同周期第一电离能自左而右具有增大趋势,所以第一电离能O>C。由于氮元素原子2p能级有3个电子,处于半满稳定状态,能量较低,第一电离能大于相邻元素,所以元素X、Y、Z的第一电离能由大到小的顺序为N>O>C。
(3)根据晶胞结构并依据均摊法可知,晶胞Mg原子的个数=8× =1个;Ni原子的个数=6×
=1个;Ni原子的个数=6×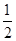 =3个;碳原子的个数=1个,所以其化学式为MgNi3C。由于顶点被周围的8个正方体共用,所以根据晶胞结构可判断一个Mg原子紧邻(3×8)÷2=12个Ni原子。
=3个;碳原子的个数=1个,所以其化学式为MgNi3C。由于顶点被周围的8个正方体共用,所以根据晶胞结构可判断一个Mg原子紧邻(3×8)÷2=12个Ni原子。
4)R的氢氧化物Ni(OH)2能溶于含CN-离子的溶液生成一种配离子[Ni(CN)4]2-,其中CN-是配体,因此反应的离子方程式是Ni(OH)2+4CN-=[Ni(CN)4]2-+2OH-。HCN分子中含有1个碳氢单键和1个碳氮三键,由于单键是σ键,三键是由1个σ键与2个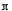 键构成的,所以化合物HCN分子中存在的σ键与
键构成的,所以化合物HCN分子中存在的σ键与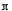 键的数目之比为2:2=1:1。
键的数目之比为2:2=1:1。
本题难度:一般
3、选择题 下列说法不正确的是( )
A.含有共价键的化合物必是共价化合物
B.化学反应中一定有化学断裂,同时也有化学键形成
C.含有阴离子的化合物一定含有阳离子
D.金属元素和非金属元素形成的化合物不一定是离子化合物
参考答案:A
本题解析:
本题难度:简单
4、简答题 下列物质中,只存在离子键的是______,只存在共价键的是______;含离子键和非极性键的是______,属于离子化合物的是______,属于共价化合物的是______.(以上各空都填序号)
①N2②MgCl2③NH4Cl?④CH4⑤CO2⑥Ne?⑦H2S?⑧KOH?⑨Na2O2?⑩K2O.
参考答案:①N2只存在共价键;
②MgCl2只存在离子键,属于离子化合物;
③NH4Cl含离子键、极性共价键,属于离子化合物;
?④CH4只存在共价键,属于共价化合物;
⑤CO2只存在共价键,属于共价化合物;
⑥Ne不存在化学键;
?⑦H2S只存在共价键,属于共价化合物;
?⑧KOH含离子键、极性共价键,属于离子化合物;
?⑨Na2O2含离子键、非极性共价键,属于离子化合物;
?⑩K2O只存在离子键,属于离子化合物;
故答案为:②⑩;①④⑤⑦;⑨;?②③⑧⑨⑩;④⑤⑦
本题解析:
本题难度:一般
5、填空题 氧元素与多种元素具有亲和力,所形成化合物的种类仅次于碳元素。
(1)氮、氧、氟元素的第一电离能从大到小的顺序为?,氧元素与氟元素能形成OF2分子,该分子的空间构型为?。
(2)根据等电子原理,判断NO2+离子中,氮原子轨道的杂化类型为?,1molO22+所含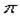 键的数目为?。
键的数目为?。
(3)氧元素与过渡元素可以形成多种价态的金属氧化物。如铬可生成Cr2O3、CrO3等,试写出Cr3+核外电子排式?。
(4)钙在氧气中燃烧时得到一种钙的氧化物晶体,其结构如图所示: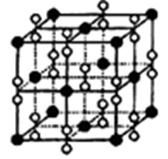
由此可判断该钙的氧化物的化学式为?。已知晶胞边长为540pm,则该氧化物的密度是?g・cm-3。
参考答案:(1)F ?N? O? V
(2)sp? 2NA
(3)[Ar]3d3或1s22s22p63s23p63d3
(4)CaO2;3.04g/cm3
本题解析:(1)第一电离能由大到小顺序是FNO,由于O中的孤电子对对数=(6-2×1)/2=2,所以OF2分子的空间构型是V形。
(2)NO2+与CO2是等电子体,所以N是sp杂化;O22+离子与N2互为等电子体,1molN2中含有2mol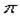 ,故1molO22+所含
,故1molO22+所含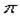 键的数目2NA。
键的数目2NA。
(3)Cr是24号元素,所以Cr3+的核外电子排布式是[Ar]3d3或1s22s22p63s23p6d3
(4)该晶胞结构与NaCl结构相似,所以它的化学式为CaO2,密度=4×72/(NA ×5403×10-30)= 3.04g/cm3。
本题难度:一般