时间:2017-03-05 13:39:08
1、填空题 把50ml?2mol?L-1的NaCl溶液稀释成100ml,稀释后NaCl的物质的量浓度为______.
参考答案:令稀释后氯化钠的物质的量为cmol/L,根据稀释定律,稀释前后溶质氯化钠的物质的量不变,则:
50mL×2mol?L-1=100mL×cmol/L,
解得c=1,
故答案为:1mol/L.
本题解析:
本题难度:一般
2、选择题 下列叙述正确的是( )
A.某可溶性物质的摩尔质量大于18g/mol,则该物质的浓溶液的密度一定大于1g/cm3
B.某温度时,NaCl饱和溶液的质量分数为a%,NaCl的溶解度为Sg,则a一定大于S
C.将90%的H2SO4溶液与10%的H2SO4溶液等体积混合,所得混合溶液中H2SO4的质量分数一定等于50%
D.饱和KCl溶液的密度为ρg/cm3,物质的量浓度为cmol/L,则此溶液中KCl的质量分数为
| 74.5c 1000ρ |
参考答案:A.因溶解度、浓度不确定,不能计算密度,则可溶性物质的摩尔质量大于18g/mol,则该物质的浓溶液的密度不一定大于1g/cm3,故A错误;
B.饱和溶液中S100+S×100%=a%,则S大于a,故B错误;
C.浓硫酸的浓度越大,其密度越大,则混合溶液的质量分数为ρ1×V×90%+ρ2×V×10%ρ1×V+ρ2×V,ρ1>ρ2,则H2SO4的质量分数小于50%,故C错误;
D.c=1000ρw%M,则饱和KCl溶液的密度为ρg/cm3,物质的量浓度为cmol/L,则此溶液中KCl的质量分数为74.5c1000ρ?100%,故D正确;
故选D.
本题解析:
本题难度:简单
3、选择题 在配制一定物质的量浓度的NaOH溶液时,下列原因可能会造成所配溶液浓度偏高
[? ]
参考答案:B
本题解析:
本题难度:一般
4、实验题 如下图为配制250mL0.2mol·L-1 Na2CO3 溶液的示意图:
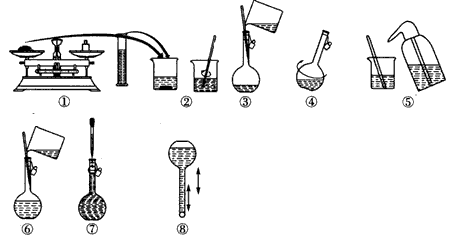
参考答案:(1)5.3
(2)搅拌 ;引流
(3)偏高 ;偏低
本题解析:
本题难度:一般
5、选择题 已知某饱和溶液的以下条件:①溶液的质量?②溶剂的质量?③溶液的体积?④溶质的摩尔质量?⑤溶质的溶解度?⑥溶液的密度,其中不能用来计算该饱和溶液的物质的量浓度的组合是?
[? ]
A、④⑤⑥?
B、①②③④?
C、①③④?
D、①③④⑤
参考答案:C
本题解析:
本题难度:简单