时间:2017-03-03 00:13:56
1、选择题 已知在298K时下述反应的有关数据:
C(s)+1/2O2(g) === CO(g) △H1= -110.5 kJ·mol-1
C(s)+O2(g) === CO2(g) △H2= -393.5 kJ·mol-1
则C(s)+CO2(g) ===2CO(g) 的△H 为
[? ]
A.+283.5 kJ·mol-1
B.+172.5 kJ·mol-1
C.-172.5 kJ·mol-1
D.-504 kJ·mol-1
参考答案:B
本题解析:
本题难度:一般
2、填空题 由金红石(TiO2)制取单质Ti,涉及的步骤为:已知: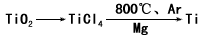
①C(s)+O2(g)====CO2(g) ΔH=-393.5 kJ·mol-1
②2CO(g)+O2(g) ====2CO2(g) ΔH=-566 kJ·mol-1
③TiO2(s)+2Cl2(g) ====TiCl4(s)+O2(g) ΔH=+141 kJ·mol-1
则
(1)TiO2(s)+2Cl2(g)+2C(s) ====TiCl4(s)+2CO(g)的ΔH=____________________。
(2)碳在氧气中不完全燃烧生成CO的热化学方程式为_______________________________。
参考答案:(1)-80kJ·mol-1
(2)C(s)+1/2O2(g)==CO(g) ΔH=-110.5 kJ·mol-1
本题解析:
本题难度:一般
3、选择题 已知热化学方程式:
①?C2H2(g)?+?5/2O2(g)?==?2CO2(g)+H2O(l)?ΔH1=-1301.0?kJ·mol-1
②?C(s)+?O2(g)?==?CO2(g)?△H2=-393.5?kJ·mol-1
③?H2(g)+?1/2O2(g)?==?H2O(1)?△H3?=?-285.8?kJ·mol-1
则反应④?2C(s)+?H2(g)?==?C2H2(g)的△H为
[? ]
A.?+228.2?kJ·mol-1?
B.?-228.2?kJ·mol-1?
C.?+1301.0?kJ·mol-1?
D.?+621.7?kJ·mol-1
参考答案:A
本题解析:
本题难度:一般
4、填空题 填空并写出下列反应的热化学方程式:
(1)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂过氧化氢,当它们混合时,即产生大量氧气和水蒸气,并放出大量热。已知0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65kJ的热量。
①写出肼和过氧化氢的电子式:? 肼___________,过氧化氢___________?。
②写出热化学方程式________________________。
③已知H2O(1)=H2O(g)?△H=+44kJ/mol,则64g液态肼与足量液态过氧化氢反应生成氮气和液态水时,放出的热量是_________?kJ。
(2)NA表示阿伏加德罗常数,在CH4(g)完全燃烧生成CO2和液态水的反应中,每有
4NA个电子转移时,放出445kJ的热量。 _______________________________
(3)已知拆开1molN≡N键,1molH-H键,1molN-H键分别需要的能量是a?kJ、b?kJ、c?kJ,则N2与H2反应生成NH3的热化学方程式为: ______________________________
(4)已知:
N2(g)+2O2(g)===2NO2(g)?ΔH=+67.7?kJ/mol①
N2H4(g)+O2(g)===N2(g)+2H2O(g)?ΔH=-543?kJ/mol②
1/2H2(g)+1/2F2(g)===HF(g)?ΔH=-269?kJ/mol③
H2(g)+1/2O2(g)===H2O(g)?ΔH=-242?kJ/mol④
①写出肼(N2H4)和NO2反应的热化学方程式_____________________________________。
②有人认为若用氟气代替二氧化氮作氧化剂,则反应释放的能量更大,肼和氟气反应的热化学方程式为_________________________________。
参考答案:(1)①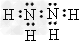 ;
; ;②N2H4(1)+2H2O2(1)=N2(g)+4H2O(g)?△H=-641.625kJ/mol
;②N2H4(1)+2H2O2(1)=N2(g)+4H2O(g)?△H=-641.625kJ/mol
③1635.25?
(2)CH4(g)?+?2O2(g)?=?CO2(g)?+?2H2O(l)?△H=?-890kJ/mol
(3)N2(g)?+?3H2(g)?=?2NH3(g)?△H=?-(6c-?a-3b)kJ/mol
(4)2N2H4(g)+2NO2(g)?===3N2(g)+4H2O(g)?ΔH=-1153.7?kJ/mol
N2H4(g)+2F2(g)?===N2(g)+4HF?(g)?ΔH=-1135?kJ/mol
本题解析:
本题难度:一般
5、选择题 化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差,参考下表键能数据和晶体硅与二氧化硅结构模型估算晶体硅在氧气中燃烧生成二氧化硅晶体的热化学方程式:Si(s)+O2(g)=SiO2(s)中,△H的值为( )
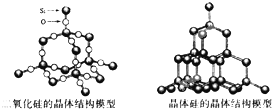
参考答案:A
本题解析:
本题难度:简单