时间:2017-03-02 23:43:16
1、选择题 设NA为阿伏加德罗常数的数值,下列叙述中正确的是?
A.3.4gNH3中含有电子数为0.2NA
B.标准状况下,22.4 L Cl2参加所有化学反应转移的电子数一定都是2NA
C.标准状况下,0.5NA个SO3分子所占的体积约为11.2 L
D.在18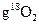 中含有
中含有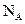 个氧原子
个氧原子
2、填空题 标准状况下,336 L的NH3溶于1L水中,所得溶液的溶质质量分数为______________,若该溶液的密度为ag/cm3,则其物质的量浓度为____________________。将上述氨水全部转化为NH4Cl,所需4 mol/L的盐酸的体积为________________________。
3、选择题 标准状况下,ag气体A和bg气体B的分子数相同,下列说法不正确的是
A.气体A和B的相对分子质量之比为 a:b
B.同质量的气体A和B所含分子数目之比为b:a
C.标准状况下,气体A和B的密度之比为b:a
D.相同条件下,等体积的气体A和B的质量之比为a:b
4、计算题 .(12分)由等物质的量的 和
和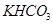 组成的混合物18.400 g,与100 mL盐酸反应。(题中涉及的气体体积均为标准状况下,填空时可以用带字母的式子表示。)
组成的混合物18.400 g,与100 mL盐酸反应。(题中涉及的气体体积均为标准状况下,填空时可以用带字母的式子表示。)
(1)该混合物中 与
与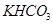 的质量分别为 和 。
的质量分别为 和 。
(2)若碳酸氢盐与盐酸恰好完全反应,则盐酸的物质的量浓度为  。
。
(3)如果盐酸过量,生成 的体积为 L。
的体积为 L。
(4)如果反应后碳酸氢盐有剩余,盐酸不足量,要计算生成 的体积,还需要知道 。
的体积,还需要知道 。
(5)若 和
和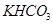 不是以等物质的量混合,则18.4 g固体混合物与足量的盐酸完全反应时生成
不是以等物质的量混合,则18.4 g固体混合物与足量的盐酸完全反应时生成 的物质的量(用n表示)的范围是 。
的物质的量(用n表示)的范围是 。
5、填空题 实验室用氯化钠固体配制1.00 mol/L的NaCl溶液0.5 L,回答下列问题:
(1)请写出该实验的实验步骤:
① ,② ,③ ,④ ,⑤ ,⑥ 。
(2)所需仪器为:托盘天平、还需要那些实验仪器才能完成该实验,请写出: 。
(3)试分析下列操作对所配溶液的浓度有何影响及造成该影响的原因。
定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。对所配溶液浓度的影响: ,原因是: 。