时间:2017-03-02 23:43:16
1、计算题 把2.0 mol・L-1 CuSO4和1.0 mol・L-1 H2SO4溶液等体积混合(假设混合后的溶液的体积等于混合前两种溶液的体积之和)
计算:
(1)混合溶液中CuSO4和H2SO4的物质的量浓度 c(CuSO4)=_________; c(H2SO4)=_________。
(2)混合液中H+ 和SO42-的物质的量浓度 c(H+)= ________; c(SO42-)= _________。
(3)向溶液中加入铁粉,经过足够长的时间,铁粉有剩余。此时溶液中Fe2+的物质的量浓度,c(Fe2+)=___________。
参考答案:(1) c(CuSO4)=1.0 mol/L ;c(H2SO4) =0.5 mol/L
(2) c(H+)=1.0 mol/L ;c(SO42-)=1.5 mol/L
(3) c(Fe2+)=1.5 mol/L
本题解析:
本题难度:一般
2、选择题 从1L1 mol/L的NaOH溶液中,取出50mL溶液,该50mL NaOH溶液的物质的量浓度为
A.0.02mol/L
B.0.2mol/L
C.1 mol/L
D.2mol/L
参考答案:C
本题解析:溶液的浓度和它的体积无关,从某溶液中取出一定体积的溶液,其浓度不会发生改变,故浓度还是1 mol/L ,选C。
考点:溶液物质的量浓度的理解。
本题难度:一般
3、选择题 0.012kg14C含有的碳原子数
A.等于NA
B.小于NA
C.大于NA
D.无法判断
参考答案:B
本题解析:14C的质量数为14,所以其相对原子质量可近似看作是14,所以0.012kg14C的物质的量是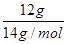 <1mol,因此答案是B。
<1mol,因此答案是B。
本题难度:一般
4、填空题 同温同压同体积的氨气(NH3)水蒸气(H2O)的分子数之比?,质量之比为?;同质量的氨气和水蒸气的体积之比为?,其中含有的氢原子个数之比为?;若二者氢原子数相等,则他们的体积之比为?。
参考答案:1:1? 17:18? 18:17? 27:17? 2:3
本题解析:略
本题难度:简单
5、填空题 (9分)
(1)3.6g H2O的物质的量是________,含有________mol H。
(2)在标准状况下,4g H2、11.2 L O2、1mol H2O中,所含分子数最多的是________,质量最大的是________。(填化学式)
(3)等质量的二氧化硫和三氧化硫,它们的物质的量之比为________,所含的硫原子数之比为________,所含的氧原子数之比为________。
(4)下列物质:①H2O? ②石墨? ③NH4NO3? ④硫酸? ⑤CH3COOH? ⑥蔗糖属于弱电解质的是?;属于非电解质的是?(用编号填写)。
参考答案:(1)0.2mol 0.4? (2)H2 H2O (3)5∶4 5∶4 5∶6(4)①⑤? ⑥
本题解析:(1)3.6gH2O的物质的量为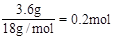 ,含有0.4molH。
,含有0.4molH。
(2)标准状况下,4gH2的物质的量为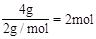 ,11.2LO2的物质的量为
,11.2LO2的物质的量为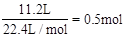 ,质量为16g,1molH2O的质量为18g。因此含分子数最多的是H2。质量最大的是H2O。
,质量为16g,1molH2O的质量为18g。因此含分子数最多的是H2。质量最大的是H2O。
(3)等质量的二氧化硫和三氧化硫,它们的物质的量之比为5∶4;所含的硫原子数之比为5∶4;所含的氧原子数之比为5∶6。
(4)弱电解质为:水、醋酸。非电解质为:蔗糖。
点评:电解质和非电解质都属于化合物,单质或混合物既不是电解质也不是非电解质。电解质主要包含酸碱盐和金属氧化物,非电解质主要包含有机物和大部分的非金属氧化物。强电解质包含强酸、强碱和大部分的盐类,弱电解质包含弱酸、弱碱和水。
本题难度:一般