时间:2017-03-02 22:39:05
1、填空题 下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
| ?主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 2 ① ② ③ 3 ④ ⑤ ⑥ ⑦ ⑧ 4 ⑨ ⑩ |
参考答案:(1)元素⑩位于第四周期第ⅦA族,应为溴元素,故答案为:溴;第四周期第ⅦA族;
(2)元素的非金属性越强,其对应的最高价氧化物的水化物的酸性越强,由于F元素无正价,则最高价氧化物的水化物的酸性最强的化合物应是HClO4,元素的金属性越强,则对应的最高价氧化物的水合物的碱性越强,在以上元素中,金属性最强的元素为K元素,对应的KOH的碱性最强,其电子式为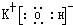
,故答案为:HClO4;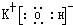
;
(3)元素④为Na元素,⑥为S元素,形成的化合物为Na2S,为离子化合物,用电子式表示元素Na与S的化合物的形成过程
为:
,故答案为:
;离子;
(4)上述元素组成的既有离子键又有非极性共价键的物质为Na2O2、K2O2等,故答案为:Na2O2或K2O2;
(5)⑥为S元素、⑦为Cl元素、⑨为K元素,三种元素形成的离子原子核外电子排布相同,原子核外电子排布相同的离子,原子序数越大,半径越小,则有离子半径S2->Cl->K+,故答案为:S2->Cl->K+.
本题解析:
本题难度:一般
2、填空题 (10分)A、B、C、D、E、F、G七种元素的原子序数依次递增。已知:
①G的原子序数为29,其余的均为短周期主族元素;
②A是宇宙中含量最多的元素,B原子最外层电子数是次外层电子数的2倍,C原子核外有三个未成对电子;
③D和E原子价电子排布式均为ns2np4;④F的单质是黄绿色气体。
请回答下列问题:
(1)G2+的核外电子排布式是?。在[G(NH3)4]2+离子中,G2+与NH3分子形成的是?键。
(2)与B、C形成的阴离子(BC―)互为等电子体的微粒有?、?(分子和离子各写一种)。
(3)B与C形成的化合物中,下列判断正确的是?。
a.氢化物稳定性:B>C? b.氢化物沸点:B<C
c.最高价氧化物的水化物酸性:B<C?d.非金属性:B>C
(4)B、C、D第一电离能由小到大的顺序为?(用元素符号作答),B的一种氢化物相对分子质量为26,分子中的σ键与π键数目比为?。
(5)七种元素中,电负性最大的元素与B元素形成化合物电子式为?,该物质的晶体属于?。
参考答案:(第三问2分,其余每空1分)? (1)1s22s22p63s23p63d9?配位
(2)N2、CO、C22-、O22+、NO+等? (3)bc? (4)C<O<N? 3:2? (5) 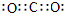 ?分子晶体
?分子晶体
本题解析:G的原子序数为29,则G是铜。A是宇宙中含量最多的元素,所以A是O。B原子最外层电子数是次外层电子数的2倍,则B是碳元素。F的单质是黄绿色气体,因此F是Cl。D和E原子价电子排布式均为ns2np4,所以根据原子序数大小可知,D是O,E是S。又因为C原子核外有三个未成对电子,所以C是N。
(1)根据构造原理可知,G2+的核外电子排布式是1s22s22p63s23p63d9;铜离子和氨气分子能形成配位键。
(2)价电子数和原子数分别都相等的是等电子体,因此与B、C形成的阴离子CN―互为等电子体的微粒有N2、CO、C22-、O22+、NO+等。
(3)非金属性压强,氢化物的稳定性越强。氮元素的非金属性强于碳元素的,所以氢化物稳定性是B<C,a和d都不正确;氨气分子间存在氢键,沸点高于甲烷的,b正确;非金属性压强,最高价氧化物的水化物的酸性越强,c正确,答案选bc。
(4)非金属性越强,第一电离能越大。但由于氮元素的2p轨道电子属于半充满状态,稳定性强,所以第一电离能大小顺序是C<O<N。相对分子质量为26的碳元素的氢化物是乙炔,分子中含有碳碳三键。单键都是σ键,三键是由1个σ键和2个π键构成的,所以乙炔分子中的σ键与π键数目比为3:2。
(5)七种元素中,电负性最大的元素是氧元素,和碳元素形成的化合物是CO2,含有极性键,电子式是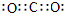
,该物质的晶体属于分子晶体。
点评:该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。本题基础性较强,重点突出,难度不大。
本题难度:一般
3、选择题 下列说法中正确的是
[? ]
A.双原子分子中化学键键能越大,分子越牢固
B.双原子分子中化学键键长越长,分子越牢固
C.双原子分子中化学键键角越大,分子越牢固
D.同一分子中,σ键要比π键的分子轨道重叠程度一样多,只是重叠的方向不同
参考答案:A
本题解析:
本题难度:一般
4、填空题 金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。
(1)写出Ti基态原子的电子排布?。
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物。则电负性C?B(选填“>”“<”),第一电离能N>O,原因是?。
(3)月球岩石玄武岩的主要成分为钛酸亚铁(FeTiO3)。FeTiO3与80%的硫酸反应可生成TiOSO4。SO42-的空间构型为?,其中硫原子采用?杂化,氧原子的价电子排布图为?,任意写出一种SO42-等电子体?。
(4)将TiOSO4的稀溶液加热水解后,经进一步反应,可得到钛的某种氧化物。该氧化物的晶胞结构图如图所示。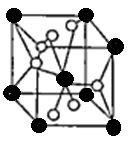
则该氧化物的化学式?(图中钛原子用“O”表示。氧原子用“O”表示)
参考答案:(1)1s22s22p63s23p63d24s2
(2)>? N原子2p上处于半充满状态,比较稳定,所以第一电离能N>O
(3)正四面体;sp3?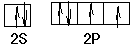 ?CCl4或ClO4-或S2O32-或PO43-
?CCl4或ClO4-或S2O32-或PO43-
(4)TiO2
本题解析:(1)Ti是22元素,核外电子排布式是1s22s22p63s23p63d24s2
(2)非金属性越强,电负性越大,所以电负性C大于B;N原子2p上处于半充满状态,比较稳定,所以第一电离能N>O;
(3)SO42-是AB4型,原子的孤对电子对数是(6+2-4×2)/2=0,所以立体构型是正四面体,采取sp3杂化;氧原子价电子是6,其价电子排布图是, ,与SO42-互为等电子体是5个原子,价电子数是32个,因而符合的有CCl4或ClO4-或S2O32-或PO43-;
,与SO42-互为等电子体是5个原子,价电子数是32个,因而符合的有CCl4或ClO4-或S2O32-或PO43-;
(4)O的个数是4×1/2+2=4,Ti的个数是8×1/8+1=2,该晶体的化学式为TiO2。
本题难度:一般
5、选择题 下列说法正确的是
A.由C、H、O、N四种元素组成的化合物一定是离子化合物
B.ⅠA族除氢元素外的所有元素的金属性比ⅡA族元素的金属性强
C.含有最高价元素的化合物不一定具有很强的氧化性
D.化学键存在于原子之间,也存在于分子之间
参考答案:C
本题解析:A、可能组成有机化合物,为共价化合物;
B、不一定,比如Ba的金属性比Li的金属性强;
C、正确,比如Na2CO3;碳+4价,最高价,没有有氧化性;
D分子间的为分子间作用力;不是化学键
本题难度:一般