�о�Ũ�ȶԷ�Ӧ���ʵ�Ӱ��
?
�ο��𰸣�C
���������
���������A�����ݽ����������������ŵ���Ⱥ�˳������жϽ������ǿ����ͭ�����ȷŵ磬����ͭ��Ծ�������ȷ��B�����ݡ�Խ��Խˮ�⡱����ˮ����ɣ���ۺ����������Խ�����Ӧ���������ˮ��̶�Խ��pHԽ��һ���Ƴ���ǽ�����Խ������ȷ��C����pH��ֽ�ⶨŨ��Ϊ0��1mol��L��1NaClO��������ֽƯ�ף�ʵ��ﲻ��Ŀ�ģ�����D�����Ƶ�һ���������ı�Ũ�ȣ��ܹ��ﵽʵ��Ŀ�ģ���ȷ��
�����Ѷȣ�һ��
2������� ��ˮ�������Ƹ����������ȵ�600��㿪ʼ�ֽ⣬�ֽ���������ƺ�����һ�ֹ��壮ijѧ������ˮ�����������Ⱥ����������ˮ�Ƴ�Ũ��Һ������ͼ��ʾ��ʵ��װ�ý���ʵ�飬����������Һ�л�������μ���ϡ���ᣬ����ʵ�������жϹ�����������ʲô�ɷ֣�����֪��Na2?S+2HCl�T2NaCl+H2S+SO2+2H2S�T3S+2H2?O��
��1����ˮ�����������ȷֽ�Ļ�ѧ����ʽ��______��װ���е�NaOH��Һ��������______��
��2����������¶���600�����ϣ��������ù����������Һ�л����μ�ϡ�������������۲쵽CuSO4��Һ�г��ֺ�ɫ�������Է�������װ���п��ܳ��ֵ�����������Һ��______������������������ӷ���ʽ��______��Ʒ����Һ��______���������������ԭ���ǣ�______��
��3����������������ϡ�����Ʒ����Һ��CuSO4��Һ���������Ե���������ԭ����______��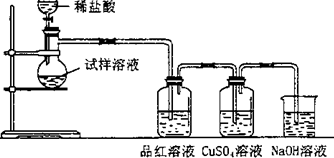
�ο��𰸣���1������������600�����Ͽɷֽ⣬������ѧ��ѧ��δ���ܣ���
���������
�����Ѷȣ�һ��
3��ʵ���� ��ͼ�����������Ҵ�����������������ļ����ʵ��װ�á��ɹ�ѡ����Լ��У�����ͭ��ĩ���Ҵ�������������������Һ��������Һ����ˮ�����������Һ��������������ѡ����������װ���ڿ����Ĵ��ڣ�
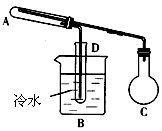
��1�����Ҵ�����ʵ��ʱ��C��Ӧװ___________________��
��2����_________�����ȣ�ʵ��һ��ʱ���A����ʵ������___________________��
��3���ڼ����Ҵ���������ʱ����B��D�ľ����������Ϊ___________________�����з�Ӧ�Ļ�ѧ����ʽΪ___________________��
�ο��𰸣���1���ƾ�
��2��AC�������ɺڱ�죨�ܿ���Һ�Σ�<
���������
�����Ѷȣ�һ��
4��ʵ���� ijѧ����ͼ�õ�ⷨ���ݵ缫�����������ʵ��������ⶨ�����ӵ�����ֵ����ʵ�鷽����Ҫ��Ϊ��
����ֱ�������Ȼ�ͭ��Һ������������ͼ��
���ڵ���ǿ��ΪI���࣬ͨ��ʱ��Ϊt���Ӻ�ȷ���ij�缫��������ͭ������Ϊm�ˡ�
�Իش�
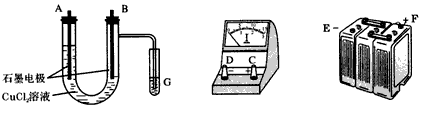
(1)������Щ��������ȷ˳��Ϊ����ͼ�б�ע������������Ӣ����ĸ��ʾ��E��____��C��____��____��F��
(2)д��B�缫�Ϸ�����Ӧ�����ӷ���ʽ____________��G�Թ��е���KI��Һ�仯������Ϊ____________����Ӧ�����ӷ���ʽ��____________________
(3)Ϊ��ȷ�ⶨ�缫������ͭ���������������ʵ�鲽����Ⱥ�˳��Ӧ��_____��ѡ�����в�������ı�ţ���
�ٳ������ǰ�缫�������ڹ��µ���缫�ϵ�ͭ����ϴ����������ˮ��ϴ����缫��
�ܵ��º�ɵ缫��������ݵ��º�ɹ��µ�ͭ����������ٴε��º�ɺ���������ء�
(4)��֪���ӵĵ���Ϊ1.6��10-19���ء����г������ӵ������ļ������ʽ��NA=____________��
�ο��𰸣�(1)D��A��B
(2)2Cl--2e-=Cl2������
���������
�����Ѷȣ�һ��
5��ѡ���� ��ͼ����ȡ��ϴ�Ӳ������������������װ��ʾ��ͼ,���ø�װ�ý����±�����ʵ�飬�ܴﵽʵ��Ŀ�ĵ��� ��???��
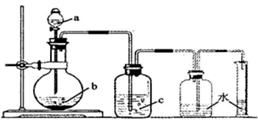
 ���� ����
ʵ��
| a��Һ�壩
| b(����)
| c(Һ��)
| A
| ϡ����
| �
| ŨH2SO4
| B
| ϡ����
| ʯ��ʯ
| ŨH2SO4
| C
| Ũ����
| CuƬ
| NaOH��Һ
| D
| ϡHNO3
| CuƬ
| H2O
?
�ο��𰸣�A
�����������
�����Ѷȣ���
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա��ҵ���ʦ��������40G
|