时间:2017-01-24 18:10:05
1、选择题 0.1mol/LNaOH溶液和0.1mol/LNH4Cl溶液等体积混合后,溶液中离子浓度关系正确的是
A.c(NH4+)+ c(H+) =c(OH-)
B.c(Na+)=c(Cl-)>c(H+)=c(OH-)
C.c(NH4+)+c(NH3・H2O) =2c(Cl-)
D.c(NH4+) >c(NH3・H2O)>c(OH-)>c(H+)
参考答案:A
本题解析:根据电荷守恒可知c(NH4+)+ c(H+) +c(Na+)=c(Cl-)+c(OH-) ,而c(Na+)=c(Cl-),所以选项A正确,B不正确,C中应该是c(NH4+)+c(NH3・H2O) =c(Cl-),D应该是c(NH4+) <c(NH3・H2O),答案选A。
本题难度:简单
2、选择题 下列热化学方程式中的△H,属于燃烧热的是[???? ]
A. H2(g)+1/2O2(g)=H2O(g)△H=-241.8 kJ/mol
B. H2(g)+Cl2(g)=2HCl(g) △H=-184.6kJ/mol
C. 2CO(g)+O2(g)=2CO2(g) △H= -566 kJ/mol
D. C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) △H=-1 366 kJ/mol
参考答案:D
本题解析:
本题难度:简单
3、填空题 (4分)
(1)用0.1mol/L NaOH溶液分别中和pH和体积均相同的盐酸和醋酸,消耗NaOH溶液的体积较多的是?????????。
(2)已知NaHCO3水溶液呈碱性,则其溶液中五种离子的浓度由大到小的顺序是(用规范的浓度符号回答)??????????????????????????????????????????。
参考答案:(1)醋酸;(2)c(Na+)>c
本题解析:(1)醋酸是弱酸,在pH相同的情况下,醋酸的浓度等于盐酸的,所以醋酸消耗的氢氧化钠多。
(2)NaHCO3水溶液呈碱性,说明其水解程度大于电离程度。又因为水还能电离出氢离子,所以浓度由大到小的顺序是c(Na+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-)。
本题难度:简单
4、选择题 (7分) t℃时,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,则:
(1)该温度下,水的离子积常数kw=??????????????。
(2)在该温度下,将100mL0.1mol/L的稀硫酸与100mL0.4mol/L的NaOH溶液混合后,溶液的pH=????????。
3)该温度下,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是????????????????。
(4)该温度下,pH=2的某酸HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。试分析其原因???????????????????????????????????????????????????????????????。
参考答案:(1)10-12???(2)11??(3)a+b = 14<
本题解析:(1)稀溶液中氢离子和OH-的浓度之积是水的离子积,所以kw=c(H+)・c(OH-)=10-a・10-b=10-a-b=10-12。
(2)根据数据可判断氢氧化钠是过量的,所以反应后c(OH-)=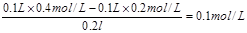 则c(H+)=
则c(H+)=本题难度:一般
5、选择题 2008年北京奥运会“祥云”火炬用的是环保型燃料――丙烷(C3H8),悉尼奥运会火炬所用燃料为65%丁烷(C4H10)和35%丙烷,已知丙烷的燃烧热为: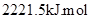 -1,下列有关说法正确的是(???)
-1,下列有关说法正确的是(???)
A.奥运火炬燃烧主要是将化学能转变为热能和光能
B.丙烷的沸点比正丁烷高
C.丙烷、空气及铂片可组成燃料电池,在丙烷附近的铂极为电池的正极
D.丙烷燃烧的热化学方程式为C3H8(g)+5O2(g)=3CO2(g)+4H2O(g);△H=-2221.5kJ/mol
参考答案:A
本题解析:丙烷的碳原子数小于丁烷的,所以沸点低于丁烷的,B不正确。原电池负极失去电子,所以丙烷再负极通入,C不正确。燃烧热是指再一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时放出的热量,水的稳定状态是液态,D不正确,答案选A。
本题难度:一般