时间:2017-01-19 10:21:33
1、选择题 下列说法不正确的是
A.CO2、甲烷都属于温室气体
B.用甘蔗生产的乙醇燃料属于可再生能源,利用乙醇燃料不会产生温室气体
C.太阳能、风能和生物能源属于新能源
D.太阳能电池可将太阳能直接转化为电能
2、填空题 (6分)已知:(a)2H2(g)+O2(g)=2H2O(g) △H = -Q1
(b)2H2(g)+O2(g)=2H2O(1) △H = -Q2
(c)2CO(g)+O2(g)=2CO2(g) △H = -Q3
(1)Q1 (填>、=、<)Q2,因为 。
(2)CO和H2分别燃烧生成CO2和H2O(g),欲得到相同的热量,所需CO和H2的体积比是: 。
3、选择题 下列关于热化学反应的描述中正确的是[???? ]
A.HCl和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol
B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=2×283.0kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
4、选择题 下列物质能促进水的电离的是
A.小苏打
B.醋酸
C.乙醇
D.氯化钠
5、填空题 利用太阳能分解水产生H2,在催化剂作用下H2与CO2反应合成CH3OH,并开发出直接以甲醇为燃料的燃料电池。已知:H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ・mol-1、CH3OH(l)+ 3/2O2(g)= CO2 (g)+ 2H2O(l)?ΔH=-726.5 kJ・mol-1、CO(g) +1/2O2(g)= CO2 (g)?ΔH=-283.0 kJ・mol-1。
请回答下列问题:
⑴用太阳能分解18g水,需要消耗的能量为??????????kJ。
⑵ 液态CH3OH不完全燃烧生成CO和液态H2O的热化学方程式为?????????????。
⑶CO2合成燃料CH3OH是碳减排的新方向。在容积为2 L的密闭容器中,充2 mol CO2和6 mol H2,由CO2和H2合成甲醇,反应式:CO2(g)+3H2(g) CH3OH(g)+H2O(g),在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300 ℃):
CH3OH(g)+H2O(g),在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300 ℃):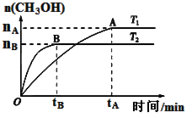
①下列说法正确的是???????????
A.温度为T2时,从反应开始到平衡,生成甲醇的平均速率为:? v(CH3OH)=nB/tB?mol・(L・min)-1
B.T2>T1,T2平衡时,甲醇产量变少,所以该反应为放热反应
C.该反应在T2时的平衡常数比T1时的平衡常数大
D.处于A点的反应体系从T1变到T2,平衡逆向移动
②能判断该反应已达化学反应限度标志的是????????(填字母。
A.H2的百分含量保持不变
B.容器中CO2 浓度与H2浓度之比为1: 3
C.容器中混合气体的密度保持不变
D.CO2消耗速率与CH3OH生成速率相等
⑷科学家致力于CO2的“组合转化”技术研究,如将CO2和H2以体积比1∶4比例混合通入反应器,适当条件下,反应可获得一种能源。完成以下化学方程式,就能知道该种能源。
CO2+4H2 2H2O + ????????。
2H2O + ????????。
⑸ 在直接以甲醇为燃料的燃料电池中,电解质溶液为酸性,总反应式为:2CH3OH + 3O2=2CO2+4H2O,则正极的反应式为?????????????;负极的反应式为????????????。