时间:2017-01-17 23:39:16
1、实验题 (10分)向溴水中加入足量乙醛溶液,可以观察到溴水褪色。对产生该现象的原因有如
下三种猜想:①溴水与乙醛发生了取代反应;②溴水与乙醛发生了加成反应③溴水将乙醛氧化成乙酸。为探究哪一种猜想正确,一研究性学习小组提出了如下两种实验方案:
方案一:检验褪色后溶液的酸碱性
方案二:测定反应前溴水中Br2的物质的量和反应后Br-的物质的量
(1)方案一是否可行??????,理由???????????????????????????????????????
(2)假设方案二中测得反应前溴水中Br2的物质的量为a mol,若测得反应后n(Br-)=
????????mol,说明溴水与乙醛发生了取代反应;若测得反应后n(Br-)=???????mol,说明溴水与乙醛发生了加成反应;若测得反应后n(Br-)=???????mol,则说明溴水将乙醛氧化成乙酸。
2、实验题 某铝合金中含有单质铝、镁、铜、硅,为了测定该合金中铝的含量,设计了如下实验流程,请回答有关问题:
(1)步骤1所得固体甲的成分为?????????????????。
(2)步骤2中加足量盐酸,而不采用通入足量二氧化碳的原因为??????????????????????????????????????????????????????????????????????。
(3)步骤3中生成固体丙的离子方程式为???????????????????????????????????;溶液C中所含有的阳离子符号为????????????????。
(4)步骤4所发生反应的化学方程式为?????????????????????????????????????。
(5)现用托盘天平称取10.0g铝合金进行上述流程图所示操作,所得固体丁质量为15.3g,则该铝合金中铝的质量分数为??????????????????;并判断以下操作对铝质量分数测定的影响(填“偏大”、“偏小”或“无影响”)。
a.步骤1中烧碱量不足,则????????????????;
b.步骤4中灼烧不充分,则????????????????。
3、实验题
某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去).实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO.由此得出的结论是浓硝酸的氧化性强于稀硝酸.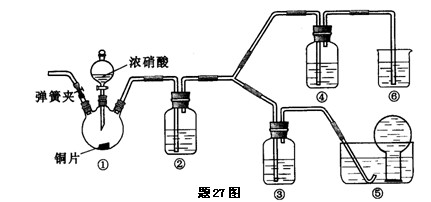
可选药品:浓硝酸、3mol/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应.2NO2+2NaOH=NaNO3+NaNO2+H2O (1)装置①中发生反应的离子方程式是???????????????????????????????????????.
(2)装置②的目的是????????????????????????????????,发生反应的化学方程式是???????????????????????????????????????????????????????????????????????.
(3)实验应避免有害气体排放到空气中,装置③、④、⑤、⑥中盛放的药品依次是
?????????????????????????????????????????????????????????????????????.
(4)实验的具体操作是:先检验装置的气密性,再加入药品,然后打开弹簧夹,通入
???????????目的是????????????????????????????????????????????????????.
(5)该小组得出的结论所依据的实验现象是???????????????????????????????????.
4、填空题 开源节流是应对能源危机的重要举措.
(1)下列做法有助于能源“开源节流”的是______(填字母).
a.大力开采煤、石油和天然气以满足人们日益增长的能源需求
b.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
c.开发太阳能、水能、风能、地热等新能源、减少使用煤、石油等化石燃料
d.减少资源消耗,增加资源的重复使用、资源的循环再生
(2)氢能是理想的清洁能源.下列制氢的方法中,最节能的是______(填字母).
a.电解水制氢:2H2O
|