时间:2017-01-16 16:09:38
1、选择题 1mol白磷转化为红磷时放出18.39kJ热量,已知:P4(白磷,s)+5O2(g)═2P2O5(s)△H=-a?kJ/mol(a>0);4P(红磷,s)+5O2(g)═2P2O5(s)△H=-b kJ/mol(b>0),则a和b的关系是( )
A.a>b
B.a=b
C.a<b
D.无法确定
2、填空题 火箭发射时可用肼(N2H4)为燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气。已知
N2(g) + 2O2(g) =2NO2(g) △H=+67.7 kJ/mol
N2H4(g) +O2(g) =N2(g) + 2H2O (g) △H = -534 kJ/mol
则N2H4和NO2反应的热化学方程式为_____________________________
3、选择题 已知:
H2O(g)== H2O(l) △H1==Q1 kJ/mol
C2H5OH(g)==C2H5OH(l) △H2==Q2 kJ/mol
C2H5OH(g)+ 3O2(g)== 2CO2(g)+ 3H2O(g) △H3==Q3kJ/mol
若使用23g酒精液体完全燃烧,最后恢复到室温,则放出的热量为 [???? ]
A、Q1+Q2+Q3
B、0.5(Q1+Q2+Q3)
C、0.5(Q1-Q2+Q3)
D、1.5Q1-0.5Q2+0.5Q3
4、选择题 由金红石(TiO2)制取单质Ti,涉及到的部分步骤为: 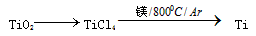
已知:
① C(s)+O2(g)=CO2(g) DH1
② 2CO(g)+O2(g)=2CO2(g) DH2
③ TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) DH3
则反应TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的DH为
[???? ]
5、简答题 (1)真空碳热还原-氯化法可实现由铝土矿制备金属铝,相关反应的热化学方程式如下:
Al2O3(s)+AlCl3(g)+3C(s)═3AlCl(g)+3CO(g)△H=a?kJ-mol-1
3AlCl(g)═2Al(l)+AlCl3(g)△H=b?kJ-mol-1
①反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H=______kJ-mol-1(用含a、b的代数式表示).
②Al4C3是反应过程中的中间产物.Al4C3与盐酸反应(产物之一是含氢量最高的烃)的化学方程式为______.
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:
Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64.39kJ-mol-1
2H2O2(aq)═2H2O(l)+O2(g)△H=-196.46kJ-mol-1
H2(g)+
| 1 2 O2(g)═H2O(l)△H=-285.84kJ-mol-1 则H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为______. |