时间:2017-01-13 10:12:43
1、填空题 为了确定HCl、C6H5OH及H2CO3的酸性强弱,有人设计了如图所示的装置进行实验:
(1)若锥形瓶中装有适量易溶于水的正盐固体,则A中发生反应的离子方程式为:______.
(2)装置B中盛放的试剂是______,它的作用是______.
(3)装置C中盛放的试剂是______,实验中观察到C中出现的主要现象是______,发生反应的方程式是______.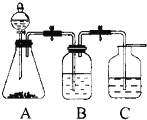
2、实验题 (13分)根据镁与二氧化碳的反应推测,钠也能在二氧化碳中燃烧,且固体产物可能为碳酸钠、氧化钠、碳中的两种或三种。某兴趣小组用如下装置开展两个阶段的实验探究。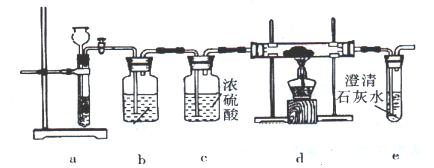
I、引发CO2与Na反应。操作步骤为:①按图连接装置,检验气密性,并往各装置中加入试剂;②打开装置a上活塞一段时间;③点燃d处酒精灯,使CO2与Na充分反应。停止加热,继续通气体使双通直管冷却。回答下列问题:
(1)操作①时,装置b中装入的试剂是???????????;
(2)步骤②时,当观察到?????????时,才能进入步骤③。
Ⅱ:探究反应产物及反应机理。取反应后双通管中固体物质29.2g进行如下实验:
①仔细观察固体,发现有黑色颗粒;
②将固体溶于足量的水并过滤、洗涤,得到1.8 g滤渣(干燥);
③将滤液加水稀释配成250ml的溶液;
④取少量③的溶液,先加足量BaCl2溶液,再加酚酞试液,观察到白色沉淀及溶液变红;
⑤取25.0mL③的溶液,用3.0mol·L-1盐酸滴定,消耗盐酸20.00mL。回答下列问题:
(3)反应后装置d中的固体物质为???????????
(4)通过计算分析:29.2g残留固体中,各组分的质量各是多少?
(5)该探究条件下,钠与二氧化碳反应的化学方程式为???????。
3、实验题 (16分)Fe、Cu都是人类较早使用的金属,某校化学研究性学习小组的同学运用实验的手段研究Fe、Cu以及化合物的相关性质。请你参与研究并回答下列问题:
(1)甲同学完成了Fe、Cu分别与S、Cl2反应的实验,下列物质中不可能为甲同学实验得到的生成物是???????
A.FeCl3
B.FeCl2
C.CuCl2
D.FeS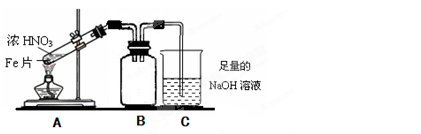
(2)乙同学为验证Fe能和热的浓HNO3反应,设计了如上图所示的实验装置,请说出装置B的作用:??????????????????????????????。开始加热前????????(填“有”或“无”)明显现象。
(3)当乙同学实验结束时,铁完全溶解,试管液面上方为无色气体,试管上部为红棕色气体,此时丙同学用所得的溶液进行如下实验和探究:
①在所得的溶液中加入一小块Cu片,结果Cu片先逐渐溶解,并伴随其他现象,反应一段时间后不再溶解。丙同学依据反应现象得出Cu片溶解的原因可能是和过量的HNO3发生反应。他依据的反应现象是????????????????????????????????????????????????????????;该反应的离子方程式为??????????????????????????????。你认为Cu片溶解是否还有另一原因,若有请用化学方程式表示其理由:????????????????????????????????(若无此空不填)
②请你设计实验证明在加入Cu片并反应完全后的溶液中含有Fe2+但不含有Fe3+。说明具体的操作和实验现象??????????????????????????????????????????????????????????。
③丙同学实验结束后加水稀释后得到溶液500mL,假设实验全过程硝酸只被还原成NO和NO2共0.02 mol并测得溶液中Fe2+和Cu2+浓度均为0.02 mol/L,则NO3-的物质的量浓度为???
mol/L。生成NO气体的体积为 _________________L(标准状况)。
(4)本次探究实验用掉密度为1.5g·cm-3质量分数为95%的浓硝酸3mL,超出实际参加反应的量其原因有(写出两点):①??????????????????????????②???????????????????
4、选择题 随着现代化学的发展,出现了各种分析和测试物质结构、跟踪化学反应过程的技术。下列不属于现代化学研究重要手段的是[???? ]
A.X-射线????
B.天平????
C.质谱????
D.核磁共振
5、实验题 (10分)为了测定乙醇的分子结构,有人设计了图甲所示的用无水乙醇与钠反应并测定H2的体积的实验装置。回答下列有关问题: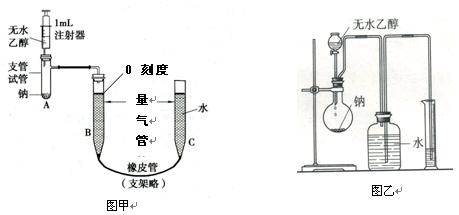
(1)乙醇与钠反应方程式为:__________________________________________________。
(2)按图将仪器装配好,降低C管,使B、C两管间出现15~20cm水位差异后停止。该操作的目的是?????????????????????????????。
(3)已知无水乙醇密度为0.789g/mL,现取0.5mL无水乙醇,将0.25mL无水乙醇慢慢推入A中,使之与钠充分反应,则A中至少应加入钠的质量为?????。(小数点后保留一位数字)
(4)注射器中吸入0.5mL无水乙醇,将称好的钠放入A中,在将乙醇推入A中之前应该进行的操作是????????????????????????????????????????????????????????????。
(5)也有人设计了如图乙所示的测定乙醇的分子结构的装置。试分析实验装置甲与实验装置乙相比,优点有???????????????????????????????????(填出两点即可)。