ʱ��:2017-01-12 20:32:23
1��ѡ����  ?? ��H����1.9 kJ/mol
?? ��H����1.9 kJ/mol
C(s�����ʯ)��O2(g)��CO2(g)����H1
C(s��ʯī)��O2(g)��CO2(g)����H2
����������Ӧ��ʵ���ó��Ľ�����ȷ����
[???? ]
2������� ��Դ��ȱ������������ٵ��ش����⡣�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��1����ҵ��һ������������ַ�Ӧ�ϳɼ״���
��ӦI�� CO(g)��2H2(g)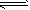 CH3OH(g) ��H1
CH3OH(g) ��H1
��ӦII��CO2(g)��3H2(g)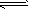 CH3OH(g) + H2O(g) ��H2
CH3OH(g) + H2O(g) ��H2
���±����������Ƿ�ӦI�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����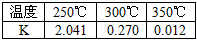
�ɱ��������жϦ�H1______0 �����������������������
��ij�¶��£���2 mol CO��6 mol H2����2L���ܱ������У�5min��÷�Ӧ�ﵽƽ�⣬���c(CO)��0.2
mol/L������H2��ʾ�ĸ÷�Ӧ�ķ�Ӧ����Ϊ��________����ʱ���¶�Ϊ________�����ϱ���ѡ��
��2����֪�ڳ��³�ѹ�£�
�� 2CH3OH(l) �� 3O2(g) ��2CO2(g) �� 4H2O(g) ��H ����1275.6 kJ/mol
�� 2CO (g)+ O2(g) ��2CO2(g) ��H ����566.0 kJ/mol
�� H2O(g) ��H2O(l) ��H ����44.0 kJ/mol
д���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ��______________________
��3��ijʵ��С�����ݼ״�ȼ�յķ�Ӧԭ���������ͼ��ʾ�ĵ��װ�á� 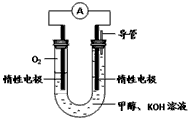
�ٸõ�������ĵ缫��ӦΪ__________________��
���øõ�ص��200mL����ʳ��ˮ(��������)��һ��ʱ��������ñ��������2.24L��������Һ��pHΪ________����Һ����仯���Բ��ƣ���Ҫʹ������Һ��ԭ����������Ϊ___________�������ƣ���
3������� ��1����֪
��CO(g) + 1/2 O2(g) =CO2(g) ��H1= -283��0 kJ/mol
��H2(g) + 1/2 O2(g) = H2O(l) ��H2= -285��8 kJ/mol
��C2H5OH(l) + 3O2(g) = 2CO2(g) + 3H2O(l) ��H3=-1370 kJ/mol
�Լ����2CO(g)�� 4H2(g)= H2O(l)��C2H5OH(l) �Ħ�H4______________
��2�����ӣ�Ni-Cd���ɳ�������ִ��������й㷺Ӧ�ã����ӿɳ�����еĵ������ҺΪKOH��Һ��Cd(OH)2��Ni(OH)2��NiO(OH)��������KOH��Һ�����ij�ŵ練Ӧ����ʽ����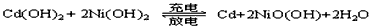
��ֱ�д���õ���ڷŵ缰���ʱ�ĵ缫��Ӧʽ��
____________________________________
4��ѡ���� ��ѧ��Ӧ�ġ�H���ڷ�Ӧ�ж��Ѿɻ�ѧ���ļ���֮���뷴Ӧ���γ��»�ѧ���ļ���֮�͵IJ�ο��±��������ݺ;�������������ṹģ���㾧�����������ȼ�����ɶ������辧����Ȼ�ѧ����ʽ��Si��s��+O2��g��=SiO2��s���У���H��ֵΪ��������
| ��ѧ�� | Si-O | O�TO | Si-Si | Si-Cl | Si-C ����kJ?mol-1 460 498.8 176 360 347 |