时间:2025-06-26 02:42:14
1、选择题 根据化学平衡知识,判断下列 说法正确的是(?)
说法正确的是(?)
A.已知NaHA溶液呈弱碱性,则该溶液中下列各种微粒浓度大小排列顺序为:
c(Na+)>c(HA-)>c(A2-)>c(H2A)
B.在小苏打溶液中存在下列关系:c(HCO3-)=c(Na+)-c (CO32-)-c(H2CO3)
C.向AgCl悬浊液中加入足量的NaI溶液,无明显现象产生
D.常温下,稀释0.1 mol/L的氨水,溶液中所有离子浓度均下降
参考答案:B
本题解析:略
本题难度:一般
2、选择题 某二元酸(简写为H2A)溶液,按下式电离: H2A=H++HA- HA-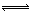 H++A2-,已知常温下浓度为0.1mol/L的H2A溶液中c(H+)=0.11mol/L,则关于0.1mol/L的NaHA溶液的下列叙述中正确的是:(?)
H++A2-,已知常温下浓度为0.1mol/L的H2A溶液中c(H+)=0.11mol/L,则关于0.1mol/L的NaHA溶液的下列叙述中正确的是:(?)
A.溶液肯定不显中性,但显酸性还是碱性无法确定
B.常温下0.1mol/L的NaHA溶液的PH=2
C.溶液中c(Na+)=c(HA-)+ c(A2-)
D.溶液中c(Na+)>c(HA-)>c(A2-)>c(H+)
参考答案:C
本题解析:由电离方程式可以知道H2A的一级电离为强电离,二级电离为弱电离,所以HA-不发生水解,只发生电离,电离显酸性所以NaHA溶液显酸性,A错误;由于HA-的电离是弱电离所以无法计算常温下0.1mol/L的NaHA溶液中的氢离子浓度,无法确定PH的具体值,B错误;根据NaHA溶液中的元素守恒可以知道钠元素与A元素的浓度之比为1:1,所以c(Na+)=c(HA-)+ c(A2-),C正确;NaHA溶液中,HA-电离出的H+和A2-浓度相等,但是考虑水电离出H+所以c(H+)>c(A2-),D错误;答案选C。
本题难度:简单
3、选择题 Na2CO3水溶液中存在CO32-?+?H2O HCO3-?+OH-平衡。下列说法不正确的是
HCO3-?+OH-平衡。下列说法不正确的是
[? ]
A.稀释溶液,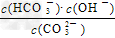 增大?
增大?
B.通入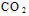 ,溶液pH减小
,溶液pH减小
C.升高温度,此平衡常数增大?
D.加入NaOH固体,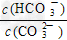 减小
减小
参考答案:A
本题解析:
本题难度:一般
4、选择题 下列物质的水溶液,pH大于7的是
A.SO2
B.NH3
C.NH4Cl
D.Na2SO4
参考答案:B
本题解析:略
本题难度:简单
5、填空题 一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式存在;钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中。
从废料中回收氧化钴(CoO)的工艺流程如下: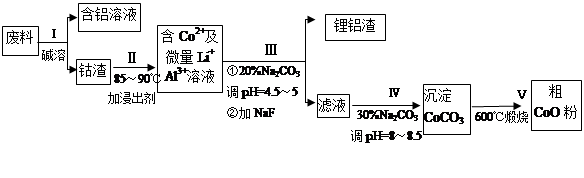
(1)过程I中采用NaOH溶液溶出废料中的Al,反应的离子方程式为?。
(2)过程Ⅲ得到锂铝渣的主要成分是LiF和Al(OH)3,碳酸钠溶液在产生Al(OH)3时起重要作用,请写出该反应的离子方程式________?____________。
(3)碳酸钠溶液在过程III和IV中所起作用有所不同,请写出在过程IV中起的作用是?。
(4)在Na2CO3溶液中存在多种粒子,下列各粒子浓度关系正确的是___?___(填序号)。
A.c(Na+) = 2c(CO32-)
B.c(Na+) > c(HCO3-) > c(CO32-)
C.c(OH-) > c(HCO3-) > c(H+)
D.c(OH-) - c(H+) = c(HCO3-) + 2c(H2CO3)
(5)CoO溶于盐酸可得粉红色的CoCl2溶液。CoCl2含结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水。下图是粉红色的CoCl2·6H2O晶体受热分解时,剩余固体质量随温度变化的曲线,A物质的化学式是______。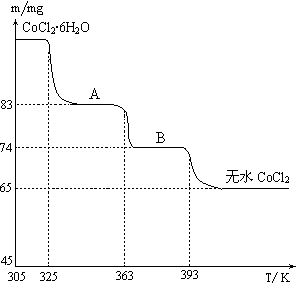
参考答案:(1)2Al+2OH-+2H2O = 2AlO2-+3H2↑
(2)2Al3++3CO32-+3H2O = 2Al(OH)3↓+3CO2↑
(3)调整pH,提供CO32-,使Co2+沉淀为CoCO3
(4)C? D (有错不得分,答对1个得1分,全对得2分)
(5)CoCl2?2H2
本题解析:(1)铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,反应的离子反应方程式为:2Al+2OH-+2H2O=+2AlO2-+3H2↑;(2)铝离子能与碳酸根离子发生双水解生成氢氧化铝和二氧化碳,水解的离子方程式为:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑;(3)碳酸钠溶液在过程Ⅲ中铝离子能与碳酸根离子发生双水解生成氢氧化铝和二氧化碳;碳酸钠溶液在过程Ⅳ中调整pH,提供CO32-,使Co2+沉淀为CoCO3;(4)A、Na2CO3溶液中电荷守恒:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-),故A错误;B、碳酸根离子发生水解以及水的电离,所以溶液中离子浓度:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+),故B错误;C、碳酸根离子发生水解以及水的电离,所以溶液中离子浓度:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+),故C正确;D、Na2CO3溶液中质子守恒:c(H+)═c(OH-)+c(HCO3-)+2c(H2CO3),故D正确。
故选:CD;
(6)CoCl2?6H2O~CoCl2
238? 130?
m?65mg
238 / m =130 /65mg?解得:m=119mg
A物质的化学式为CoCl2?nH2O,则有:
CoCl2?6H2O~CoCl2?nH2O△m
238? 18(6-n)
119mg?119mg-83mg
238 /119mg =18(6?n)/119mg?83mg,解得:n=2,
所以A物质的化学式为:CoCl2?2H2O。
本题难度:困难