时间:2025-06-26 02:30:48
1、填空题 (8分)某反应中反应物与生成物有:KClO3、K2SO4、H2C2O4、CO2、H2SO4、H2O和一种氧化物X。
(1)已知KClO3在反应中得到电子,则该反应的还原剂是?。
(2)已知0.2 mol KClO3在反应中得到0.2 mol电子生成X,则X的化学式为?。
(3)根据上述反应可推知?(填字母编号)。
a.氧化性:KClO3> CO2? b.氧化性:CO2> KClO3
c.还原性:H2C2O4>X? d.还原性:X> H2C2O4
(4)写出该反应的离子方程式:?。
2、选择题 已知:
①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;
②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色;
③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色
下列判断正确的是
[? ]
A.上述实验证明氧化性:MnO4- >Cl2>Fe2+ >I2
B.上述实验中,共有两个氧化还原反应
C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝
D.实验②证明Fe2+既有氧化性又有还原性
3、选择题 金属加工后的废切削液中含2―5%的NaNO2,它是一种环境污染物。人们用NH4Cl溶液来处理此废切削液,使NaNO2转化为无毒物质。该反应分两步进行:
第一步:NaNO2+NH4Cl=NaCl+NH4NO2?第二步:NH4NO2= N2↑+2H2O
下列对第二步反应的叙述中正确的是(? )
①NH4NO2是氧化剂?② NH4NO2是还原剂?③ NH4NO2发生了分解反应
④只有氮元素的化合价发生了变化?⑤ NH4NO2既是氧化剂又是还原剂
A.①③
B.①④
C.②③④
D.③④⑤
4、选择题 日常生活中的许多现象都与化学反应有关,下列现象与氧化还原反应无关的是(?)。
A.铁制菜刀生锈
B.酸雨腐蚀大理石雕像
C.铜制饰品上出现绿色斑点[Cu2(OH)2CO3]
D.铝锅表面生成致密的氧化膜
5、填空题 向盛有KL溶液的试管中加入少许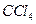 后滴加氯水,
后滴加氯水,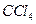 层
层 变成紫色。如果继续向试管中滴加氯水,振荡,
变成紫色。如果继续向试管中滴加氯水,振荡,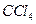 层会逐渐变浅,最后变成无色。
层会逐渐变浅,最后变成无色。
完成下列填空:
1) 写出并配平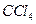
 层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):
层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):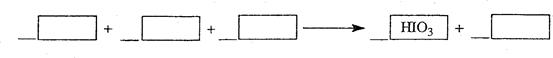
2)整个过程中的还原剂是___。
3)把KL换成KBr,则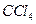 层变为__色:继续滴加氯水,
层变为__色:继续滴加氯水,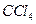 层的颜色没有变化。
层的颜色没有变化。 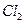 ?、
?、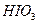 、
、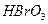 氧化性由强到弱的顺序是______。
氧化性由强到弱的顺序是______。
4)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含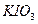 的食盐)1000kg,若庄Kl与
的食盐)1000kg,若庄Kl与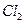 反应制
反应制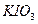 ,至少需要消耗
,至少需要消耗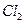 ________L(标准状况,保留2位小数)。
________L(标准状况,保留2位小数)。