时间:2025-06-26 01:50:57
1、填空题 (11分)T、X、Y、Z、Q、R、W为周期表前四周期元素,原子序数依次递增,其中某些元素的相关信息如下表:
| 元素 | 相关信息 |
| T | T原子所处的周期数、族序数分别与其原子序数相等 |
| X | X的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同 |
| Z | Z的基态原子价电子排布为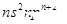 |
| Q | 在该元素所在周期中,Q的基态原子的第一电离能最小 |
| R | 3p能级上有1个电子 |
| W | W的一种核素的质量数为65,中子数为36 |
参考答案:1)N>C>Na?(2)高?(3)[Ar]3d9或1s22s22p63s23p63d9;C
(4)sp3?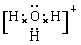 ?
? ,?极性? 2F2+2H2O=4HF+O2
,?极性? 2F2+2H2O=4HF+O2
(5)+47.2 kJ/mol(2分)
本题解析:根据元素的结构及其性质可知,T、X、Y、Z、Q、R、W分别是H、C、N、O、Na、Al、Cu。
(1)非金属性越强,电负性越大,所以X、Y、Q三种元素的电负性由大到小的顺序是N>C>Na。
(2),晶体结构与金刚石类似,石墨是原子晶体。由于碳原子半径大于氮原子半径,原子半径越小,共价键越强,所以该晶体的熔点大于金刚石的。
(3)根据构造原理可知,铜离子的电子排布式为[Ar]3d9或1s22s22p63s23p63d9。根据方程式可知,氧气是氧化剂,所以HO2是还原产物,选项C不正确,其余都是正确的,答案选C。
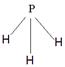
(4)A为5原子核的+1价阳离子,则A是NH4+,氮原子是sp3杂化。B为4原子核的+1价阳离子,则B是H3O+,其电子式为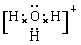 。C为4个原子核构成的分子,则C是氨气,所以与氨气互为等电子体的分子可以是PH3,其结构式为
。C为4个原子核构成的分子,则C是氨气,所以与氨气互为等电子体的分子可以是PH3,其结构式为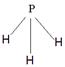 。D是双氧水,属于极性分子。E应该是是单质氟,和水反应的方程式为2F2+2H2O=4HF+O2。
。D是双氧水,属于极性分子。E应该是是单质氟,和水反应的方程式为2F2+2H2O=4HF+O2。
(5)考查盖斯定律的应用。①-②即得到3Z2(g)?2Z3(g)?△H=+283.2 kJ/mol。所以16g Z2(g)完全转化为Z3(g)的△H=+283.2 kJ/mol÷6=+47.2 kJ/mol。
本题难度:一般
2、选择题 下列式子中,真实表示物质分子组成的是?(?)
A.H2O
B.NH4Cl
C.SiO2
D.C
参考答案:A
本题解析:略
本题难度:简单
3、选择题 某晶体的一部分如下图所示,这种晶体中A、B、C三种粒子数之比是(? )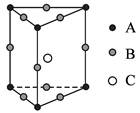
A.3∶9∶4?B.1∶4∶2? C.2∶9∶4?D.3∶8∶4
参考答案:B
本题解析:这不是一个平行六面体晶胞,而是一个正三棱柱结构,它分摊到的各个粒子数目分别为:顶点1/12,水平棱上1/4,竖直棱上1/6,面上1/2,内部1。所以A、B、C三种粒子数之比为(6×1/12)∶(6×1/4+3×1/6)∶1=1∶4∶2
本题难度:一般
4、选择题 下列物质中,分子的立体结构与水分子相似的是
[? ]
A.CO2
B.H2S
C.PCl3
D.SiCl4
参考答案:D
本题解析:
本题难度:简单
5、选择题 第三周期元素形成的单质中,属于原子晶体的是( )
A.金刚砂
B.金刚石?
C.单晶硅
D.二氧化碳
参考答案:
C
本题解析:
单质只有金刚石和单晶硅,它们都是原子晶体,但碳是第二周期元素,硅才是第三周期元素。
本题难度:一般