时间:2025-06-26 00:25:57
1、选择题 (2014届浙江省宁波市十校高三3月联考理综化学试卷)
高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是
A.铁是阳极,电极反应为Fe-6e一+4H2O=FeO42-+ 8H+
B.电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极
C.若隔膜为阴离子交换膜,则OH-自右向左移动
D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计)
2、选择题 下列说法正确的是
A.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属
B.锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后再用酸溶解去除
C.饱和Ca(OH)2溶液中加入一定量的生石灰,所得溶液的 pH 会增大
D.反应NH3(g)+HCl(g)=NH4Cl(s)△H<0在任何条件下均能自发进行
3、填空题 请分析下列有关铝盐溶液电解时的变化情况。
(1)用石墨作电极,用如图装置电解AlCl3溶液,两极均产生气泡,阴极区有沉淀生成。持续电解,在阴极附近的溶液中还可观察到的现象是?,解释此现象的离子方程式是?。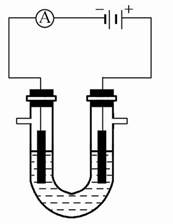
(2)若用石墨作电极电解NaCl和Al2(SO4)3的混合溶液,混合溶液中二者的物质的量浓度分别为3 mol・L-1、0.5 mol・L-1,则下列表示电解过程的曲线正确的是?。
4、选择题 (08年黄冈模拟,9)用NaOH溶液吸收二
氧化硫,将所得的混合液进行电解循环再生,这种新工艺叫再生循环脱硫法。其中阴阳膜组合循环再生机理如图,则下列有关说法正确的是(?)
A.阳极区酸性减弱
B.阴极区电极反应式为:2H++2e―=H2↑
C.该过程主要是为了获得H2SO4
D.电解时两个电极都只能用惰性材料
5、填空题 重铬酸钠俗称红矾钠(Na2Cr2O7・2H2O)是重要的化工产品和强氧化剂。工业制备的流程如下: ?
?
请回答:
(1)已知Fe(CrO2)2中铬元素是+3价,则Fe(CrO2)2中铁元素是____价。
(2)化学上可将某些盐写成氧化物的形式,如Na2SiO3可写成Na2O・SiO2,则Fe(CrO2)2可写成____。
(3)煅烧铬铁矿时,矿石中难溶的Fe(CrO2)2生成可溶于水的Na2CrO4,反应化学方程式如下: ?
?
为了加快该反应的反应速率,可采取的措施是____。
(4)已知CrO42―在不同的酸性溶液中有不同的反应,如: ?
?
①往混合溶液甲中加入硫酸必须适量的原因是____。
②混合溶液乙中溶质的化学式是____。
(5)+3、+6价铬都有很强的毒性,+6价铬的毒性更高,可诱发肺癌和鼻咽癌,所以制取红矾钠后的废水中含有的Cr2O72―必须除去。工业上可用电解法来处理含Cr2O72―的废水,下图为电解装置示意图(电极材料分别为铁和石墨)。通电后,Cr2O72―在b极附近转变为Cr3+,一段时间后Cr3+最终可在a极附近变成Cr(OH)3沉淀而被除去。
a电极的电极反应式是?,
b电极附近反应的离子方程式是?。