ʱ��:2025-06-26 00:25:57
1������� ��9�֣��������ƣ�NaClO2����һ��ǿ������Ư�����㷺���ڷ�֯��ӡȾ��ʳƷ��ҵ�����ڼ��Ի������ȶ����ڡ�ijͬѧ�������Ϻ��������NaClO2����Ҫ�������¡�
��1�����з�����Ӧ�Ļ�ԭ���ֱ��� �� ���ѧʽ����
��2�����з�Ӧ�����ӷ���ʽ�� ��
��3��A�Ļ�ѧʽ�� ��װ�â���A�� ����������
��4��ClO2��һ�ָ�Чˮ�������������������ƺ�ϡ����Ϊԭ���Ʊ���д�����Ʊ���Ӧ�Ļ�ѧ����ʽ ��
��5��NaClO2���ʿɷֽ�ΪNaClO3��NaCl��ȡ����������ǰ���NaClO2�����������Һ���ֱ�������FeSO4��Һ��Ӧʱ������Fe2+�����ʵ��� �������ͬ��������ͬ�������жϡ���
�ο��𰸣���9�֣�
(1) Na2SO3 H2O (��1��)
(2) 2ClO2 + H2O2 + 2OH��= 2ClO2-+ O2��+ 2H2O��2�֣�
(3) H2SO4 ��(��1��)
(4)5NaClO2 + 4HCl =" 5NaCl" + 4ClO2�� + 2H2O��2�֣�
(5) ��ͬ��1�֣�
��������������ƺ�������������ҺA����������ԭ��Ӧ���������ƺ�ClO2���壬��÷�Ӧ��SԪ�صĻ��ϼ����ߣ�����������������ԭ�������ɵ������ƽ�����أ���ʵ�ʱ�������ˮ������ˮ�ǻ�ԭ��Ҳ�����������������⡢ClO2���塢NaOH�������ʷ�Ӧ����NaClO2������a����ΪClԪ�صĻ��ϼ۽��ͣ����Թ���������OԪ�صĻ��ϼ����ߣ�������aΪ������������bΪ������
��1���������Ϸ��������з�����Ӧ�Ļ�ԭ���ֱ���Na2SO3�� H2O��
��2�����з�Ӧ�ǹ������⡢ClO2���塢NaOH�������ʷ�Ӧ����NaClO2������������Ԫ���غ㣬���������ˮ���ɣ����Է�Ӧ�����ӷ���ʽ��2ClO2 + H2O2 + 2OH��= 2ClO2-+ O2��+ 2H2O��
��3����ΪIII�����Ӹ�Ĥ���أ������������������ӷŵ磬����������������Ũ���������������ͨ����Ĥ���������������Բ���������һ��ͬʱ�������ᣬ����ҺA�Ļ�ѧʽΪH2SO4����������������
��4�����������ƺ�ϡ����Ϊԭ���Ʊ�ClO2��ClԪ�صĻ��ϼ���-1��+3��+4�ۣ�����������ԭ��Ӧ���ɣ������������е�ClԪ�صĻ��ϼ����ߵ�+4�ۣ�ͬʱ���͵�-1�ۣ����Բ�������ˮ���Ȼ������ɣ���ѧ����ʽΪ5NaClO2 + 4HCl =" 5NaCl" + 4ClO2�� + 2H2O��
��5��NaClO2���ʿɷֽ�ΪNaClO3��NaCl����ѧ����ʽΪ3 NaClO2=2NaClO3+NaCl���������ı���ǰ���NaClO2�����������Һʱ�����ʺ��NaClO3��NaCl������������ʱ��ʵ���ǵ�����NaClO2�����������ӣ�����+3��ClԪ�ر���ԭΪ�����ӣ�ת�Ƶ��ӵ���Ŀ��ͬ����������Fe2+�����ʵ�����ͬ��
���㣺������ȡ�������ƵĹ�ҵ���̵ķ�����������ԭ��Ӧ�ķ���
�����Ѷȣ�����
2������� ���ԭ���ڻ�ѧ��ҵ���й㷺��Ӧ�á���ͼ��ʾһ�����أ�?װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ������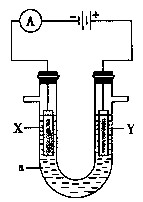
��ش��������⣺
��1����X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ����
�ٵ�����X���ϵĵ缫��ӦʽΪ?����X�������۲쵽��������?�����Һ����X�������ƶ���������??��
��Y�缫�ϵĵ缫��ӦʽΪ?��
��2����Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ����
��X�缫�IJ����� ?
��Y�缫�ĵ缫��ӦʽΪ?(˵�������ʷ����ķ�Ӧ����д����)
����Һ�е�c(Cu2+)����ǰ��� ??(��������С�����䡱)��
�ο��𰸣���1����2H2O + 2e- = H2 + 2OH-?��2H++2e-��H2���������ݲ�������Һ���? Na+��H+
��2Cl- - 2e-=Cl2
��2���پ�ͭ?��Cu-2e-=Cu2+?�۱�С
�����������1��X�缫�͵�Դ�ĸ�����������������������Һ�е������ӷŵ磬�缫��Ӧʽ��2H++2e-��H2���������ӷŵ磬�ƻ���������Χˮ�ĵ���ƽ�⣬����������Χ��Һ�Լ��ԣ�������Һ�Ժ�ɫ�����Һ����X���������������ƶ��������������ӣ�Na+��H+��Y�缫�͵�Դ����������������������Һ���������ӷŵ������������缫��Ӧʽ��2Cl-��2e-��Cl2����
��2����ͭ����ʱ����ͭ�͵�Դ����������������������ͭ�͵�Դ�ĸ���������������������ͭ���������Һ�����Ԣ�X�缫�����Ǵ�ͭ���缫��Ӧʽ��Cu2++2e-��Cu����Y�缫�����Ǵ�ͭ���缫��Ӧʽ��Cu-2e-��Cu2+����������������ʧ���ӵ�ʱ����Һ�е�Cu2+ �õ��ӣ����Ծ��������У���Һ�е�c(Cu2+)��С��
�����Ѷȣ�һ��
3������� ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�á���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
��1����X��Y���Ƕ��Ե缫��a�DZ���NaCl��Һ��ʵ�鿪ʼʱ��ͬʱ�����߸����뼸�η�̪��Һ����
�� ������X���ϵĵ缫��ӦʽΪ?����X�������۲쵽��������?��
�� Y�缫�ϵĵ缫��ӦʽΪ?������õ缫��Ӧ����ķ�����?��
��2����Ҫ�õ�ⷽ��������ͭ�����Һaѡ��CuSO4��Һ����
�� X�缫�IJ�����?���缫��Ӧʽ��?��
�� Y�缫�IJ�����?���缫��Ӧʽ��?��
��˵�������ʷ����ĵ缫��Ӧ����д����
�ο��𰸣���1���� 2H+��2e-��H2�����ų����壬��Һ���� 2Cl�C��2e-��Cl2������ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ��2���� ��ͭ��Cu2+��2e-��Cu �� ��ͭ��Cu��2e-��Cu2+
�����������1���ٺ͵�Դ�ĸ��������ĵ缫X�����������õ缫�������ӷ����õ��ӵĻ�ԭ��Ӧ����2H++2e-=H2�������Ըõ缫����������Ũ����������ǿ�����뼸�η�̪��Һ���죬�ʴ�Ϊ��2H++2e-=H2�����ų����壬��Һ��죻�ں͵�Դ�����������ĵ缫Y�����������õ缫�������ӷ���ʧ���ӵ�������Ӧ����2Cl--2e-=Cl2����������ʹʪ��ĵ⻯�ص�����ֽ�������������������ļ��飬�ʴ�Ϊ��2Cl--2e-=Cl2������ʪ��ĵ⻯�ص�����ֽ����Y�缫��������ֽ����ɫ����2���ٵ�ⷽ��������ͭ�����ص����������Ǵ�ͭ���缫��ӦΪ��Cu2++2e-=Cu���ʴ�Ϊ����ͭ��Cu2++2e-=Cu���ڵ�ⷽ��������ͭ�����ص����������Ǵ�ͭ���缫��ӦΪ��Cu-2e-=Cu2+���ʴ�Ϊ����ͭ��Cu-2e-=Cu2+��
�����Ѷȣ�һ��
4�������� (12��)��25 ��ʱ����ʯī�缫���2.0 L��2.5 mol/LCuSO4��Һ��5 min����һ��ʯī�缫����6.4 g Cu���ɡ��Իش��������⣺
��1���ж���Ħ�����ӷ���ת�ƣ��õ�O2���������״�����Ƕ�������
��2����Һ��pH�Ƕ��٣�
��3�����õ�����������ͭƬ����ʯī���缫��������ͭƬ�����������٣�
�ο��𰸣���12�֣���1��0.2mol? 1.12L?��2��1?��3��12.8g
�����������
�����Ѷȣ�һ��
5��ѡ���� �����dz�����ǿ���������㷺����ˮ����ϵͳ����ȡ�����ķ����ܶࡣ���и�ѹ�ŵ編�͵�ⴿˮ��ԭ������ͼ��ʾ�������й�˵������ȷ����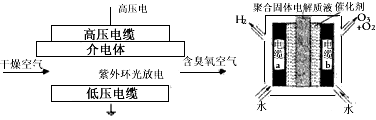
[? ]
A����ѹ�ŵ編����Ӧ��ԭ��Ϊ��3O2 2O3
2O3
B����ѹ�ŵ�����Ŀ����У�������������е���������
C����ⷨ���缫b��Χ�����ĵ缫��Ӧ�У�3H2O-6e-=O3+6H+��2H2O-4e-=O2+4H+
D�����ʱ��H+�ɵ缫a���ۺϹ�������Ĥ����缫b
�ο��𰸣�D
���������
�����Ѷȣ�һ��