时间:2025-06-26 00:18:36
1、填空题 甲醇( )是重要的能源物质,研究甲醇具有重要意义。
)是重要的能源物质,研究甲醇具有重要意义。
(1)利用工业废气中的 可制取甲醇,其反应为:
可制取甲醇,其反应为:
常温常压下已知下列反应的能量变化如图所示:
写出由二氧化碳和氢气制备甲醇的热化学方程式:
。
(2)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了 的
的  晶体,在高温下它能传导
晶体,在高温下它能传导 离子。电池工作时正极反应为 。
离子。电池工作时正极反应为 。
若以该电池为电源,用石墨做电极电解100mL含有如下离子的溶液。
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的物质的量为 mol。
(3)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后将 氧化成
氧化成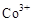 ,然后以
,然后以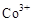 做氧化剂把水中的甲醇氧化成
做氧化剂把水中的甲醇氧化成 而净化。实验室用下图装置模拟上述过程:
而净化。实验室用下图装置模拟上述过程:
①写出阳极电极反应式 ;
②除去甲醇的离子反应为:
 ,该过程中被氧化的元素是 ,当产生标准状况下2.24L
,该过程中被氧化的元素是 ,当产生标准状况下2.24L 时,共转移电子 mol。
时,共转移电子 mol。
参考答案:(1) (2分)
(2分)
(2) (2分) 0.1(2分)
(2分) 0.1(2分)
(3)① (2分) ②C或碳(2分) 0.6(2分)
(2分) ②C或碳(2分) 0.6(2分)
本题解析:(1)左图中 转化为
转化为 时能量变化为-41 Kl·mol-1,右图中
时能量变化为-41 Kl·mol-1,右图中 转化为
转化为 时能量变化为:419 Kl·mol-1—510 Kl·mol-1= -9Kl·mol-1,则由二氧化碳和氢气制备甲醇的能量变化为-41 Kl·mol-1+(-9Kl·mol-1)=—50 Kl·mol-1
时能量变化为:419 Kl·mol-1—510 Kl·mol-1= -9Kl·mol-1,则由二氧化碳和氢气制备甲醇的能量变化为-41 Kl·mol-1+(-9Kl·mol-1)=—50 Kl·mol-1
(2)为提高甲醇燃料的利用率,在燃料电池的一个电极通入空气,此时空气作为正极,而甲醇气体作为负极,正极反应式为: 。当两极收集到相同体积(相同条件)的气体时,说明电解过程分别产生了O2、Cl2、H2,则此时阳极上收集到氧气的物质的量为0.1mol。
。当两极收集到相同体积(相同条件)的气体时,说明电解过程分别产生了O2、Cl2、H2,则此时阳极上收集到氧气的物质的量为0.1mol。
(3)由题意,通电后将 氧化成
氧化成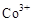 说明
说明 所在的电极为阳极,则阳极反应式为:
所在的电极为阳极,则阳极反应式为: ,CH3OH作为阴极,被氧化,其中被氧化的是甲醇中的C元素,当产生标准状况下2.24L
,CH3OH作为阴极,被氧化,其中被氧化的是甲醇中的C元素,当产生标准状况下2.24L 时,说明共产生了0.1mol
时,说明共产生了0.1mol ,则共转移电子0.6 mol。
,则共转移电子0.6 mol。
考点:化学能源、燃料电池、离子反应
点评:将有机化合物制作成相应的燃料电池,符合绿色化学与可持续发展理念,此种类型的题目为高考重要考点,体现了化学与生活息息相关,也加强了学生的化学设计与探究意识。
本题难度:一般
2、选择题 高铁电池是新型可充电电池,与普通高能电池相比,该电池放电时能长时间保持稳定的电压.高铁电池放电的化学方程式为:
3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH.下列叙述中错误的是( )
A.该反应实现了化学能向电能的转化
B.放电过程中锌元素的化合价降低
C.高铁电池能减少汞等重金属污染
D.放电过程中溶液的pH逐渐升高
参考答案:A.高铁电池放电时时化学能转化为电能的装置,故A正确;
B.放电时,Zn被氧化,化合价升高,故B错误;
C.高铁电池不含汞等重金属,可减少污染,故C正确;
D.放电时,生成KOH,溶液pH升高,故D正确.
故选B.
本题解析:
本题难度:一般
3、选择题 下图为氢氧燃料电池的原理示意图,按照此图的提示,下列叙述不正确的是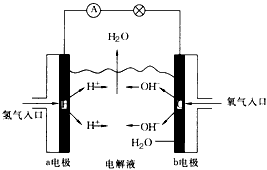
[? ]
A.a电极是负极
B.b电极的电极反应式为:4OH- -4e-=2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储存在电池内的新型发电装置
参考答案:B
本题解析:
本题难度:一般
4、选择题 一种新型燃料电池,一极通入空气,另一极通入丁烷气体,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-.下列对该燃料的说法正确的是( )
A.在熔融电解质中,O2-由负极移向正极
B.电池的总反应是:2C4H10+13O2=8CO2+10H2O
C.通入空气的一极是正极,电极反应为:O2+2e-=2O2-
D.通入丁烷的一极是正极,电极反应为:C4H10+26?e-+13?O2-=4?CO2+5?H2O
参考答案:A.原电池中,阴离子向负极移动,阳离子向正极移动,故A错误;
B.电池的总反应与丁烷燃烧的化学方程式一致,为2C4H10+13O2=8CO2+10H2O,或由正负极电极反应式判断,故B正确;
C.通入空气的一极为原电池的正极,发生还原反应,电极反应式为O2+4e-=2O2-,故C错误;
D.通入丁烷的一极是负极,电极反应式为C4H10+13O2--26e-=4CO2+5H2O,故D错误.
故选B.
本题解析:
本题难度:一般
5、选择题 爱迪生电池在充电和放电时发生的反应:Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2,下列该蓄电池推断错误的是
Fe(OH)2+Ni(OH)2,下列该蓄电池推断错误的是
[? ]
① 放电时,Fe参与负极反应,NiO2参与正极反应
② 充电时,阴极上的电极反应式为:Fe(OH)2 + 2e-= Fe + 2OH-
③ 放电时,电解质溶液中的阴离子向正极方向移动
④ 放电时,负极上的电极反应式为:Fe + 2H2O-2e- = Fe(OH)2 + 2H+
⑤ 蓄电池的电极必须浸入某种碱性电解质溶液中
A.只有③
B.③④
C.④⑤
D.①②⑤
参考答案:B
本题解析:
本题难度:一般