时间:2025-06-25 23:59:00
1、选择题 能源问题是人类社会面临的重大课题,H2、CO、CH3OH都是重要的能源物质,它们的燃烧热依次为-285.8 kJ・mol-1、-282.5 kJ・mol-1、-726.7 kJ・mol-1。已知CO和H2在一定条件下可以合成甲醇CO(g)+2H2(g)===CH3OH(l)。则CO与H2反应合成甲醇的热化学方程式为
A.CO(g)+2H2(g)===CH3OH(g) ΔH=+127.4 kJ・mol-1
B.CO(g)+2H2(g)===CH3OH(l) ΔH=+127.4 kJ・mol-1
C.CO(g)+2H2(g)===CH3OH(g) ΔH=-127.4 kJ・mol-1
D.CO(g)+2H2(g)===CH3OH(l) ΔH=-127.4 kJ・mol-1
参考答案:D
本题解析:
试题解析:CO燃烧的热化学方程式:CO(g)+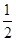 O2(g)
O2(g)
本题难度:一般
2、选择题 常温常压下,充分燃烧一定量的甲烷放出热量222.575KJ,经测定完全吸收生成的二氧化碳需消耗1mol/L的NaOH溶液250mL,恰好生成正盐。则此条件下甲烷的燃烧热热化学方程式 ( )
A.CH4(g)+2O2(g)=CO2(g)+2H2O(g);△H="-890.3" kJ/mol
B.1/2CH4(g)+O2(g)=1/2CO2(g)+H2O(l);△H="-222.575" kJ/mol
C.1/2CH4(g)+O2(g)=1/2CO2(g)+H2O(g);△H="-445.15" kJ/mol
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H="-890.3" kJ/mol
参考答案:D
本题解析:由NaOH的物质的量可以算出CO2的量,再由CO2的量算出甲烷的量,计算出1mol CH4充分燃烧放出的热量为890.3 kJ,则甲烷的燃烧热热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H="-890.3" kJ/mol。
本题难度:一般
3、选择题 在常温下10mL pH=10的KOH溶液中,加人一定量的pH=4的一元酸HA溶液至pH刚好等于7,则对反应后溶液的叙述正确的是(? )?
A.c(HA)+c(A-)=10-4mol/L? B.c(H+)=c(OH-)<c(K+)<c(A-)
C.V总≤20mL? D.酸和碱一定恰好中和
参考答案:C
本题解析:如果HA为强酸,等体积恰好中和,呈中性,V总=20mL;如果为弱酸,酸的浓度远大于碱的浓度。总体积小于20ml。
本题难度:一般
4、选择题 下列说法或表示正确的是
[? ]
A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由单质A转化为单质B是一个吸热过程,由此可知单质B比单质A稳定
C.稀溶液中:H+(aq)+OH-(aq)==H2O(l);△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含lmol
NaOH的溶液混合,放出的热量大于57.3kJ
D.在101kPa时,H2燃烧的热化学方程式为2H2(g)+O2(g) = 2H2O(l);△H=-571.6kJ/mol,则H2在
101kPa时的燃烧热为571.6kJ/mol
参考答案:C
本题解析:
本题难度:简单
5、选择题 如图表示溶液中c(H+)和c(OH-)的关系,下列判断错误的是
A.两条曲线间任意点均有c(H+)×c(OH-)=Kw
B.M区域内任意点均有c(H+)<c(OH-)
C.图中T1<T2
D.XZ线上任意点均有pH=7
参考答案:D
本题解析:依图可知,曲线上的任意点均是平衡点,且温度一定,所以其水的离子积是一个常数,A正确;当c(H+)=10-7mol/L时,向上做垂线得在M区域内c(OH-)>10-7mol/L,B正确;水的电离是吸热反应,升高温度促进水的电离,c(H+)、c(OH-)及Kw都增大,所以T2>T1,C正确;XZ线上任意点表示溶液呈中性,由于各点温度不同,故PH不同,D项错误。
本题难度:一般