ʱ��:2025-06-25 23:40:11
1��ѡ���� Ԫ�ص�ԭ�ӽṹ���������ʺ������ڱ��е�λ�ã�����˵����ȷ���ǣ�������
A��Ԫ�����ڱ���λ�ڽ����ͷǽ����ֽ��߸�����Ԫ�����ڹ���Ԫ��
B��ij���Ľṹʾ���ͼΪ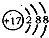
�����Ԫ�������ڱ���λ�ڵ������ڡ�VIA��
C��Be��OH��2�ļ��Ա�Mg��OH��2�ļ���ǿ
D��ԭ�Ӱ뾶��Na��Si��O
2��ѡ���� M��N��X��Y���ֶ���������Ԫ����Ԫ�����ڱ��е����λ����ͼ��ʾ����֪���ǵ�ԭ�������ܺ�Ϊ48���������й�˵���в���ȷ���� 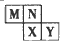
[? ]
A.N��Xλ��Ԫ�����ڱ��Т�A��
B.M��X��Y����Ԫ�ص�����������Ӧ��ˮ�����Ϊǿ��
C.M����̬�⻯����Y����̬�⻯�ﷴӦ�����������ӻ�����
D.M��N��X��Y��λ�ڽ�����ǽ����ķֽ�����
3������� �����ס�п����������������ܲ��ɷֵ�Ԫ�ء���ش��������⣺
��1�� NH3��PH3���Ǽ��Է��ӣ����м��Խϴ����______��������?��
��2�� 20mL0.1 mol��L-1�����ᣨH3PO2)��Һ��20 mL 0.1 mol��L-1 NaOH��Һǡ���к���������,��H3PO2�Ľṹʽ��?��
��3�� ��ͼ��ʾΪѪ�쵰�ͼ��쵰�Ļ��Բ��֨D�DѪ���صĽṹʽ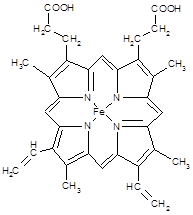 ?
?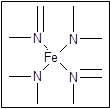
Ѫ������Nԭ�ӵ��ӻ���ʽΪ?������ͼ�ķ������á��������Fe2������λ����
��4�� N2��CO��Ϊ�ȵ����塣�±������ߵļ���
���ݣ���λ��kJ��mol-1��: 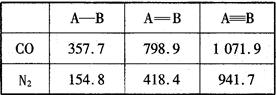
�������˵��CO��N2���õ�ԭ��_____��
��5�� Zn2+��̬ʱ�ĵ����Ų�ʽ��______��ZnO��ZnS�ľ���ṹ���ƣ������۵�ϸߵ���______��������?��
4������� ��֪��A��B��C��D��E��F����Ԫ�غ˵�����������������ڱ���ǰ�����ڵ�Ԫ�ء�����Aԭ�Ӻ���������δ�ɶԵ��ӣ�������B2E�ľ���Ϊ���Ӿ��壬Eԭ�Ӻ����M����ֻ�����ԳɶԵ��ӣ�CԪ���ǵؿ��к�����ߵĽ���Ԫ�أ�D���ʵ��۵���ͬ����Ԫ���γɵĵ�������ߣ�F���γɺ�ɫ(��ש��ɫ)��F2O�ͺ�ɫ��FO���������
�ش��������⣺
��1��F��ԭ�ӵ�M������Ų�ʽΪ?��
��2��B��C��D�ĵ�һ��������С�����˳��Ϊ?��(��Ԫ�ط��ű�ʾ)
��3��A�ļ��⻯����Ӽ�������ˮ,����Ҫԭ����?.
��4��E�������������ӵĿռ乹����?��������ԭ�ӵ��ӻ���ʽΪ?��
��5��F�ĸ�������A�ļ��⻯���γɵ�������,��λ��Ϊ?��
��6��A��F�γ�ij�ֻ�����ľ����ṹ��ͼ��ʾ�����仯ѧʽΪ?������ɫ���ʾFԭ�ӣ�,��֪���ڵİ��������֮��ľ���Ϊa cm, �þ������ܶ�Ϊ??g/cm3��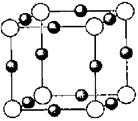
5��ѡ���� ���з����У����ں��м��Լ��ķǼ��Է��ӵ���
[? ]