时间:2025-06-25 23:19:47
1、选择题 用惰性电极电解CuSO4溶液,一段时间后取出电极。向电解后的溶液中加入9.8g的Cu(OH)2,充分反应后所得溶液与电解前相同,则
[? ]
A.电解后阳极附近溶液的pH升高
B.电解时电路中通过电子的物质的量是0.4mol
C.电解开始时阴极发生的电极反应为:2H++2e-=H2↑
D.电解时阳极发生的反应为还原反应
参考答案:B
本题解析:
本题难度:一般
2、简答题 工业上用饱和电解食盐水来制取氯气.现取500mL含NaCl为11.7g的饱和食盐水进行电解.(已知2NaCl+2H2O═2NaOH+H2↑+Cl2↑)
(1)在标准状况下制得Cl2多少升?
(2)所得NaOH的物质的量浓度为多少?(电解前后溶液体积保持不变)
参考答案:(1)根据题意,NaCl物质的量n=nM=11.7g58.5g/mol=0.2mol,
设电解过程生成氯气的物质的量为y,生成氢氧化钠的物质的量为x,
2NaCl+2H2O??通电?.??2NaOH+H2↑+Cl2↑
2? ?2? 1
0.2mol?x?y
22=0.2molx、21=0.2moly,
解得x=0.2mol、y=0.1mol,
所以在标准状况下制得Cl2体积V=nVm=0.1mol×22.4L/mol=2.24L,
答:在标准状况下制得Cl222.4L;
(2)据c=nV=0.2mol0.5L=0.4 mol/L,
答:所得NaOH的物质的量浓度为0.4 mol/L.
本题解析:
本题难度:一般
3、选择题 用惰性电极电解CuCl2和CuSO4混合溶液(浓度均为0.01摩/升)500毫升,当阴极析出0.48克Cu时,在标准状况下,阳极可得到的气体约为?
A.0.168升
B.0.14升
C.0.336升
D.0.24升
参考答案:B
本题解析:惰性电极电解CuCl2与CuSO4的混合溶液,阴极析出Cu,阳极先是2Cl--2e=Cl2,然后若还有电子转移,应为4OH--4e=2H2O+O2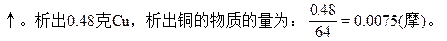
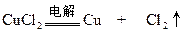
0.01×0.5? 0.005? 0.005
=0.005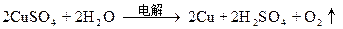
0.0075-0.005? 0.00125
=0.0025
∴阳极的气体V=(0.005+0.00125)×22.4=0.14(升)
本题难度:一般
4、选择题 已知蓄电池在充电时作电解池,放电时作原电池。铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“-”。关于标有“+”的接线柱,下列说法中正确的是
[? ]
A.充电时作阳极,放电时作正极
B.充电时作阳极,放电时作负极
C.充电时作阴极,放电时作负极
D.充电时作阴极,放电时作正极
参考答案:A
本题解析:
本题难度:简单
5、实验题 高铁酸钾(K2FeO4)具有高效的消毒作用,为一种新型非氯高效消毒剂。电解法制备高铁酸钾操作简便,成功率高,易于实验室制备。其原理如下图所示。
I.?实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。
(1)电解过程中,X极是_________极,电极反应是__________________。
(2)电解过程中,Y极放电的有_________________。
(3)生成高铁酸根(FeO42-)的电极反应是_________________。
II.?若用不同种电池作为上述实验的电源,请分析电池反应。
(1)铅蓄电池总的化学方程式为: Pb+PbO2+2H2SO4 2H2O+2PbSO4,则它在充电时的阳极反应为__________________。
2H2O+2PbSO4,则它在充电时的阳极反应为__________________。
(2)镍镉碱性充电电池在放电时,其两极的电极反应如下:
正极:2NiOOH+2H2O+2e-=2Ni(OH)2+2OH- ?
负极:Cd+2OH--2e-=Cd(OH)2
则它在放电时的总反应的化学方程式为______________________。
(3)肼(N2H4)是一种可燃性液体,可用作火箭燃料。已知在25℃、101kPa时,32.0g?
N2H4在氧气中完全燃烧生成氮气和液态水,放出624kJ的热量,则N2H4完全燃烧的热化学方程式是___________________;肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液,放电时负极的电极反应是__________________。
(4)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐,电池总反应方程式为:C3H8+5O2=3CO2+4H2O。写出该电池正极的电极反应:__________________。
(5)当制备相同物质的量的高铁酸钾时,理论上,上述四种电池中分别消耗的Pb、Cd、肼、丙烷的物质的量之比是_______________。
参考答案:Ⅰ.(1)阴;2H++2e-=?H2↑;(2)Fe和OH-;(3)Fe+8OH--6e-=?FeO42-+4H2O
Ⅱ.(1)PbSO4+2H2O-2e-=?PbO2+SO42-+4H+;(2)Cd+2NiOOH+2H2O?=?Cd(OH)2+2Ni(OH)2;(3)N2H4(l)+O2(g)=?N2(g)+2H2O(l)?△H=-624kJ/mol;N2H4+4OH--4e-=?4H2O+N2↑;(4)O2+2CO2+4e-=?2CO32-;(5)10:10:5:1
本题解析:
本题难度:一般