ʱ��:2025-06-25 21:47:33
1������� ��֪��2SO3 2SO2+O2������ʼʱ�����ͬ������A��B�У�ͬʱ�ֱ����2molSO3��������װ�д��������ڷ�Ӧ�����У�A�����¶Ⱥ��ݻ����䣻B�����¶Ⱥ�ѹǿ���䡣�ش��������⣺
2SO2+O2������ʼʱ�����ͬ������A��B�У�ͬʱ�ֱ����2molSO3��������װ�д��������ڷ�Ӧ�����У�A�����¶Ⱥ��ݻ����䣻B�����¶Ⱥ�ѹǿ���䡣�ش��������⣺
��1����Ӧ��ƽ������ʱ��A?B�����ڣ����ڣ�С�ڣ�����ƽ��ʱSO3��ת����
A?B�����ڣ����ڣ�С�ڣ���
��2����ƽ�����A��B�зֱ����������壬?������ƽ�⽫��?�����ƶ�����ƽ�����A��B�зֱ��������ʵ���SO3�����´�ƽ��ʱ���������е�SO3ת���ʱ仯����ǣ�����С�����䣩A?��B?
�ο��𰸣�
��1��С�ڣ�С�ڣ���1�֣���2�֣�
��2��B������Ӧ����С�����䣨��1�֣���4�֣�
���������
���⿼�黯ѧƽ���ƶ���2SO3 2SO2+O2����һ���������ʵ�������ķ�Ӧ����1����ͬ�¶��£�����SO3,A��������������䣬ѹǿ���B��������ѹǿ���䣬������ﵽƽ��״̬ʱת��Ϊ״̬C������ͼ��,�ʴﵽƽ������ʱ�䣬AС��B������B�еĻ������ƶ�������A��B����������������¶���ͬ���ﵽƽ��ʱA��B�������д��ڵ�ƽ���ǵ�Чƽ�⣬����SO3��ת����Ҳ��ȡ�����B��C����״̬��B��ѹǿС��C��ѹǿ�����C��SO3ת���ʴ���B��SO3ת���ʡ��ɴ˿����жϳ�C��SO3��ת����Ҳ����A��SO3��ת����, �ʴﵽƽ��ʱ��SO3��ת���� AС��B��
2SO2+O2����һ���������ʵ�������ķ�Ӧ����1����ͬ�¶��£�����SO3,A��������������䣬ѹǿ���B��������ѹǿ���䣬������ﵽƽ��״̬ʱת��Ϊ״̬C������ͼ��,�ʴﵽƽ������ʱ�䣬AС��B������B�еĻ������ƶ�������A��B����������������¶���ͬ���ﵽƽ��ʱA��B�������д��ڵ�ƽ���ǵ�Чƽ�⣬����SO3��ת����Ҳ��ȡ�����B��C����״̬��B��ѹǿС��C��ѹǿ�����C��SO3ת���ʴ���B��SO3ת���ʡ��ɴ˿����жϳ�C��SO3��ת����Ҳ����A��SO3��ת����, �ʴﵽƽ��ʱ��SO3��ת���� AС��B��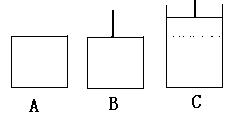
��2���ﵽƽ��ֱ����������壬A����������䣬��Ӧ��ϵ��Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���B��������ѹǿ���䣬�������ƽ�������ƶ����������SO3��A��������������䣬ѹǿ���SO3��ת���ʼ�С��B�г���SO3����ԭƽ��Ϊ��Чƽ�⣬SO3��ת���ʲ��䡣
�����Ѷȣ�һ��
2��ѡ���� ��֪��Һ�д���Cr2O72-�� H2O 2CrO42-�� 2H+��ƽ�⣬����Cr2O72-�ʳ�ɫ��CrO42-�ʻ�ɫ�����ƽ����ϵ�еμӱ���NaOH��Һʱ����ɫ�ı仯�����
2CrO42-�� 2H+��ƽ�⣬����Cr2O72-�ʳ�ɫ��CrO42-�ʻ�ɫ�����ƽ����ϵ�еμӱ���NaOH��Һʱ����ɫ�ı仯�����
A����ɫ����
B����ɫ����
C����ɫ����
D����ɫ��ȥ
�ο��𰸣�A
���������
Cr2O72-�� H2O 2CrO42-�� 2H+�����ƽ����ϵ�еμӱ���NaOH��Һʱ��H��Ũ�ȼ�С��ƽ�������ƶ�����ɫ���A��ȷ��
2CrO42-�� 2H+�����ƽ����ϵ�еμӱ���NaOH��Һʱ��H��Ũ�ȼ�С��ƽ�������ƶ�����ɫ���A��ȷ��
�����Ѷȣ���
3��ѡ���� �Կ��淴ӦN2 + 3H2 2NH3������������˵����Ӧ�Ѵ�ƽ�����?��?��?
2NH3������������˵����Ӧ�Ѵ�ƽ�����?��?��?
A����λʱ������a mol N2���ģ�ͬʱ����2a mol NH3
B��������Ũ�Ȳ��ٱ仯
C�������ڵ�����������������Ũ��֮��Ϊ1�U3�U2
D����ѧ��Ӧ���ʹ�ϵ�ǣ�2v����NH3�� = 3v�棨H2��
�ο��𰸣�B
�����������
�����Ѷȣ���
4������� ��֪2A2(g) + B2(g) 2C(g)
2C(g)  H=" -a" kJ/mol(a��0)����һ���д����Ĺ̶��ݻ����ܱ������м���2molA2��1molB2����500���dz�ַ�Ӧ�ﵽƽ���C��Ũ��Ϊw mol/L���ų�����b kJ��
H=" -a" kJ/mol(a��0)����һ���д����Ĺ̶��ݻ����ܱ������м���2molA2��1molB2����500���dz�ַ�Ӧ�ﵽƽ���C��Ũ��Ϊw mol/L���ų�����b kJ��
��1��a?b(�������=������)��
��2��������Ӧ�¶����ߵ�700�棬�÷�Ӧ��ƽ�ⳣ����?���������С�����䡱����
��3������ԭ���������У�ֻ����2mol C��500��ʱ��ַ�Ӧ�ﵽƽ�����������c kJ��C��Ũ��?w mol/L(�������=������)��a,b,c֮��������ֹ�ϵ��?(�õ�ʽ��ʾ)��
��4����˵���÷�Ӧ�Ѿ��ﵽƽ���״̬����?��
a����(C)=2��(B2)?b��������ѹǿ���ֲ���
c����(��)(A2)=��(��)(B2)? d�������ڵ��ܶȱ��ֲ���
�ο��𰸣���1���� ?��2����С?��3��=? a=b+c?��4��b
�����������1��2A2(g) + B2(g) 2C(g)
2C(g)  H=" -a" kJ/mol(a��0)����ʾ2molA��1molB��ȫ��Ӧ����2molC�ͷ�akJ����������500���dz�ַ�Ӧ�ﵽƽ��ʱ���ɵ�CС��2molC���Ƿų�����b kJ��һ��С��akJ��
H=" -a" kJ/mol(a��0)����ʾ2molA��1molB��ȫ��Ӧ����2molC�ͷ�akJ����������500���dz�ַ�Ӧ�ﵽƽ��ʱ���ɵ�CС��2molC���Ƿų�����b kJ��һ��С��akJ��
��2����Ϊ��Ӧ�� H��0,�¶�Խ�ߣ�KԽС��
H��0,�¶�Խ�ߣ�KԽС��
��3����ͬһ����ͬһ������ 2molA2��1molB2������ƽ���2mol C������ƽ��ʱ��Чƽ�⡣����ƽ���C��Ũ����Ϊw mol/L����a=b+c����4�����������ݣ���Ӧ��ȫ�������壬�����ܶ�ʼ�ղ��䣬d���У��÷�Ӧ�� Vg��0��������ѹǿ���ֲ���ʱ��˵����Ӧ�Ѵ�ƽ��״̬��b���ԣ�a�������֦�(��) =��(��)��C����AB���ʱ�ʾƽ��״̬Ӧ���Ǧ�(��)(A2)=2��(��)(B2) ��c����
Vg��0��������ѹǿ���ֲ���ʱ��˵����Ӧ�Ѵ�ƽ��״̬��b���ԣ�a�������֦�(��) =��(��)��C����AB���ʱ�ʾƽ��״̬Ӧ���Ǧ�(��)(A2)=2��(��)(B2) ��c����
�����Ѷȣ�һ��
5��ѡ���� ij�ܱ������д���2NO+O2 2NO2��Ӧ��ƽ��ʱNO��ת�������¶ȱ仯��ϵ��ͼ��ʾ(�������κ�һ�㶼��ʾƽ��״̬)������˵������ȷ����
2NO2��Ӧ��ƽ��ʱNO��ת�������¶ȱ仯��ϵ��ͼ��ʾ(�������κ�һ�㶼��ʾƽ��״̬)������˵������ȷ����
A���÷�Ӧ������Ӧ�����ȷ�Ӧ
B�����¶�ΪT1��T3ʱ��ƽ�ⳣ���ֱ�ΪK1��K3����K1��K3
C��T1ʱ������Ӧ����D�㣬��÷�Ӧ���淴Ӧ���ʴ�������Ӧ����
D�������С�����������ƽ��ʱ��ʾNOת�������¶ȱ仯��ϵ��������ԭ�����Ϸ�
�ο��𰸣�D
���������A������ͼ���֪�������¶ȵ����ߣ�NO��ת�������͡���˵�������¶�ƽ�����淴Ӧ������У��������Ӧ�Ƿ��ȷ�Ӧ��A����ȷ��B�������¶�ƽ�����淴Ӧ������У�ƽ�ⳣ�����ͣ�������¶�ΪT1��T3ʱ��ƽ�ⳣ���ֱ�ΪK1��K3����K1��K3��B����ȷ��C��T1ʱ������Ӧ����D��ʱ��Ҫ��ﵽƽ��״̬�������¶Ȳ��������£�NO��ת����������˵����Ӧ������Ӧ������У���÷�Ӧ���淴Ӧ����С������Ӧ���ʣ�C����ȷ��D�������С���������ѹǿ����ƽ��������Ӧ������У�NO��ת����������ƽ��ʱ��ʾNOת�������¶ȱ仯��ϵ��������ԭ�����Ϸ���D��ȷ����ѡD��
�����Ѷȣ���