时间:2021-06-11 07:16:12
1、实验题 (12分)某学生用标准的0.2mol/L的盐酸滴定待测的NaOH溶液,其实验操作如下:
A.用碱式滴定管取待测液NaOH溶液放入锥形瓶,滴加2―3滴酚酞指示剂。
B.用待测的NaOH溶液润洗碱式滴定管。
C.把滴定管用蒸镏水洗净。
D.取下酸式滴定管,用标准的盐酸溶液润洗后,再将标准的盐酸注入酸式滴定管至刻
度“0”以上2cm―3cm处,把酸式滴定管固定好,调节液面。
E.检查滴定管是否漏水,并分别固定在滴定管架两边。
F.另取锥形瓶,再重复滴定操作一次。
G.把锥形瓶放在酸式滴定管的下面,瓶下垫一张白纸,然后边滴定边摇动锥形瓶,直
至终点,记下滴定管的液面所在刻度。
据上述滴定操作,完成下列填空:
⑴滴定操作的正确操作顺序是(用上述各编号字母填写)
?→E→?→B→?→?→?;
⑵ G步操作中判断滴定终点的依据是?;
⑶ D步骤的操作中液面应调节到?,尖嘴部分应?;
⑷酸式滴定管未用标准的盐酸润洗,待测溶液NaOH的测定值会?;
碱式滴定管未用待测的NaOH溶液润洗,待测NaOH溶液的测定值会?。
(填“偏高”、“偏低”或“无影响”。)
参考答案:(12分)(1)(2分)C、D、A、G、F
(2)(2分)当滴加最后一滴时,锥形瓶中溶液由红色突变为无色,且半分钟内不恢复?
(3)(每空2分)刻度“0”或“0”以下;充满溶液或无气泡
(4)(每空2分)偏高;偏低
本题解析:略
本题难度:一般
2、简答题 聚合氯化铝晶体的化学式为[Al2(OH)nCl6-n?XH2O]m,它是一种高效无机水处理剂,它的制备原理是调节增大AlCl3溶液的pH,通过促进其水解而结晶析出.其制备原料主要是铝加工行业的废渣--铝灰,它主要含Al2O3、Al,还有SiO2等杂质.聚合氯化铝生产的工艺流程如下: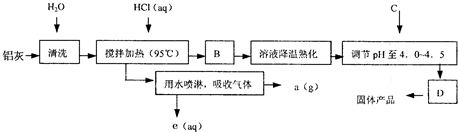
(1)搅拌加热操作过程中发生反应的离子方程式为:______;______.
(2)生产过程中B和D的操作名称分别是______和______(B和D均为简单操作).
(3)反应中副产品a是______.
(4)生产过程中可循环使用的物质是______(用化学式表示).
(5)调节pH至4.0~4.5的目的是______.
(6)实验室要测定水处理剂产品中n和x的值.为使测定结果更准确,需得到的晶体较纯净.生产过程C物质可选用______.
A.NaOH? B.Al? C.氨水? D.Al2O3 E.NaAlO2.
参考答案:(1)氧化铝与盐酸反应生成氯化铝和水,反应离子方程式为Al2O3+6H+=2Al3++3H2O;
铝与盐酸反应生成氯化铝与氢气,反应离子方程式为2Al+6H+=2Al3++3H2↑.
故答案为:Al2O3+6H+=2Al3++3H2O;2Al+6H+=2Al3++3H2↑;
(2)铝灰与过量的盐酸反应,过滤后收集滤液,加热浓缩至饱和,调pH值,稍静置,过滤收集滤渣,最终的这个滤渣就是我们要的晶体,所以生产过程中操作B和D的均为过滤.
故答案为:过滤、过滤;
(3)搅拌加热操作过程,加入盐酸,铝与盐酸反应,有氢气生成,加热的时候HCl会挥发,用水喷淋就可以吸收HCl,得到HCl(aq),剩余气体为氢气,反应中副产品a为H2.
故答案为:H2.
(4)95°C加热的时候HCl会挥发,用水喷淋就可以吸收HCl,得到HCl(aq),可进行循环使用.
故答案为:HCl;
(5)铝离子水解,Al3++3H2O?Al(OH)3+3H+,降低氢离子浓度促进铝离子水解,有利于聚合氯化铝晶体析出.
故答案为:促进AlCl3水解,使晶体析出;
(6)用氢氧化钠和氨水调节pH值,会引入新的杂质,引入钠离子和铵根离子.所以可以加入Al和氧化铝进行处理,它二者是固体,多了可以过滤掉的,所以可以使得到的晶体较纯净.
故答案为:BD.
本题解析:
本题难度:一般
3、实验题 锂离子电池的广泛应用使回收利用锂资源成为重要课题。某研究性学习小组对废旧锂离子电池正极材料(LiMn2O4和碳粉涂覆在铝箔上)进行资源回收研究,设计实验流程如下
(1)第①步反应可能产生气体的化学式是________;第②步反应得到的沉淀X的化学式为_______。
(2)第③步反应有锂离子(Li+)生成,其反应的离子方程式是___________________。
(3)四步实验都包含过滤,实验室中过滤实验要使用的玻璃仪器包括_______。
(4)若废旧锂离子电池正极材料含LiMnO4的质量为18.1 g,第③步反应中加入 20.0 mL 3.0mol/L的H2SO4溶液,假定正极材料中的锂经反应③和④完全转化为Li2CO3,则至少有______g Na2CO3参加了反应。
参考答案:(1)H2;Al(OH)3
(2)4LiMn2O4+4H++O2=8MnO2+4Li++2H2O
(3)漏斗、烧杯、玻璃棒
(4)6.4或6.36
本题解析:
本题难度:一般
4、实验题 (16分)某同学为测定黄铜矿的纯度(主要成分CuFeS2含少量SiO2),设计如下实验:称取2.0g研细的该黄铜矿样品,高温下和空气中的氧气充分反应: ? 6CuFeS2+19O2
? 6CuFeS2+19O2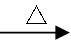 6CuO+2Fe3O4+12SO2
6CuO+2Fe3O4+12SO2
生成的SO2进入D中和水发生反应:SO2+H2O=H2SO3;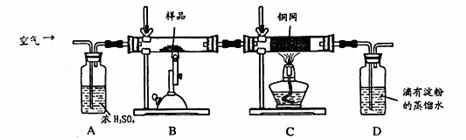
(1)称量该样品时用的仪器的名称为?。
(2)装置A的作用?;
a.有利于空气中氧 气充分反应? b.除去空气中的水份
气充分反应? b.除去空气中的水份
c.有利于气体混合? d.有利于观察空气流速
(3)装置B中反应结束后,仍需继续通一段时间空气的目的?。
(4)实验后将D中的溶液全部转移至锥形瓶,用1.0mol/L的I2溶液进行滴定,反应为:H2SO3+I2 +H2O=H2SO4+2HI,达到终点时消耗I2溶液20.00mL,判断滴定达到终点的现象为?,通过计算,该黄铜矿的纯度为?(Cu:64? Fe:56? S:32)
+H2O=H2SO4+2HI,达到终点时消耗I2溶液20.00mL,判断滴定达到终点的现象为?,通过计算,该黄铜矿的纯度为?(Cu:64? Fe:56? S:32)
参考答案:
(1)托盘天平(2分)
(2)b、d(4分,只选一个对的得2分,全对得4分,其它有错的答法不得分)
(3)使生成SO2全部进入 装置,使结果准确(2分)。除去B中多余的O2,防止其氧化D中生成的H2SO3(2分)
装置,使结果准确(2分)。除去B中多余的O2,防止其氧化D中生成的H2SO3(2分)
(4)溶液恰好由无色变成浅蓝色(2分),且半分钟内不褪色(1分) 9 2%(3分)
2%(3分)
本题解析:略
本题难度:简单
5、填空题 高铁酸钾是一种高效的多功能水处理剂,具有氧化、吸附、絮凝、、助凝、杀菌、除臭等作用,高铁酸钾的开发和利用正日益显示出其广阔的应用前景。其制备流程如下: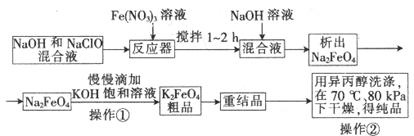
试回答下列问题
(1)反应器中,NaOH、NaClO、Fe(NO3)3发生反应生成Na2FeO4,完成并配平下列离子反应方程式:
□Fe3++□ClO─+□OH─ ==□FeO42─+□Cl─+□___________
(2)次氯酸钠浓度对高铁酸钾产率有一定影响,当NaClO浓度为298g/L时,高铁酸钠的产率最高,此时NaClO的物质的量浓度为_______________。
(3)你认为操作①能够发生转化的原因是__________,慢慢滴加的原因的是___________。
(4)操作②如果温度过高会造成高铁酸钾的分解,高铁酸钾受热分解时生成金属氧化物和氧气,该反应的化学方程式为__________________。
(5)可以用电化学法制取Na2FeO4,其装置如图所示,则阳极的电极反应式为?;
阴极的电极反应式为______________;电解一段时间后溶OH─的浓度会_________(填“升高”、“降低”
或“不变”)。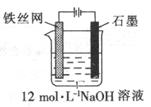
参考答案:(1) 2Fe3++3ClO─+10OH─=2FeO42─+3Cl─+5H2O
(2)4mol/L(少单位扣1分)
(3)此条件下,高铁酸钾的溶解度小于高铁酸钠的;为了使反应充分(1分)。
(4)4K2FeO4 2K2O+2Fe2O3+3O2↑(缺少条件扣1分)
2K2O+2Fe2O3+3O2↑(缺少条件扣1分)
(5)Fe+8OH-─6e-=FeO42-+4H2O;2H++2e-=H2↑(或2H2O+2e-=2OH-+H2↑);降低(1分)
本题解析:(1)根据反应可知,铁元素的化合价从+3价升高到+6价,失去3个电子。氯元素的化合价从+1价降低到-1价,得到2个电子。因此根据电子得失守恒可知,氧化剂次氯酸钠和还原剂硝酸铁的物质的量之比是3:2,根据电荷守恒可知OH-的计量数是10,根据原子守恒可知,生成物中还有水生成,所以反应的离子方程式为2Fe3++3ClO─+10OH─=2FeO42─+3Cl─+5H2O。
(2)NaClO浓度为298g/L,即1L溶液中含有次氯酸钠的质量是298g物质的量=298g÷74.5g/mol=4mol,因此次氯酸钠的物质的量浓度=4mol÷1L=4mol/L。
(3)操作1是向高铁酸钠中溶液慢慢滴加饱和氢氧化钾溶液即可以得到高铁酸钾,因此根据沉淀容易向生成更难溶的方向转化可知,在此条件下,高铁酸钾的溶解度小于高铁酸钠的;为了使反应充分小于慢慢滴加氢氧化钾饱和溶液,以提高原料利用率。
(4)高铁酸钾受热分解时生成金属氧化物和氧气,其中氧元素的化合价从-2价升高到0价,因此氧气是氧化产物,则铁元素的化合价必然降低生成氧化铁,另外还有氧化钾产生,反应的化学方程式为4K2FeO4 2K2O+2Fe2O3+3O2↑。
2K2O+2Fe2O3+3O2↑。
(5)电解池阳极失去电子,发生氧化反应。铁与电源的正极相连,做阳极,因此铁失去电子结合溶液中的OH-生成FeO42-,因此阳极电极反应式为Fe+8OH- ─6e-=FeO42-+4H2O;电解池阴极得到电子,发生还原反应,则在该电解池中溶液中的氢离子在阴极得到电子,电极反应式为2H++2e-=H2↑;根据阴阳极的电极反应式可知该电池反应的总反应方程式为Fe+2OH-+2H2O  FeO42-+3H2↑,这说明在反应过程中溶液中OH-的浓度降低。
FeO42-+3H2↑,这说明在反应过程中溶液中OH-的浓度降低。
本题难度:一般