ʱ��:2021-06-11 06:55:04
1��ѡ���� �����ʵ���Ũ�ȵ�������Һ�У�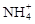 Ũ�������ǣ�?��
Ũ�������ǣ�?��
A��NH4HSO4
B��NH4Cl
C��NH4HCO3
D��NH4NO3
2������� ��֪��Һ��ֻ����OH����H����Na����CH3COO���������ӣ��Իش��������⣺
��1������Һ��ֻ�ܽ���һ�����ʣ����������?����Һ��c(H����?c(OH��)(�����������������)��
��2������Һ��c(Na��)��c(OH��)��c(CH3COO��)��c(H��)�������Һ�е�����Ϊ?������Һ��c(CH3COO��)��c(Na��)��c(H��)��c(OH��)�������Һ������Ϊ?��
��3��������Һ���������ȵ�NaOH��Һ�ʹ�����Һ��϶��ɣ���ǡ�ó����ԣ�����ǰc(NaOH��?c(CH3COOH)�����ǰ����c(OH��)������c(H��)�Ĺ�ϵc(OH����?c(H��)(�����������������)��
3��ѡ���� �������ӷ���ʽ�У�����ˮ�ⷴӦ����(? )
A��HCOOH+H2O HCOO-+H3O+
HCOO-+H3O+
B��CO2+H2O HCO3-+H+
HCO3-+H+
C��CO32-+H2O HCO3-+OH-
HCO3-+OH-
D��HS-+H2O S2-+H3O+
S2-+H3O+
4��ѡ���� �����£������и���Һ����������ȷ���ǣ�?��
A��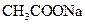 ��Һ�У�
��Һ�У�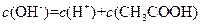

B���� ��
��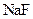 ��Һ�У�
��Һ�У�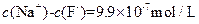
C��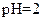 ��������
��������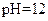 ��
�� ��Һ�������Ϻ���Һ��һ����
��Һ�������Ϻ���Һ��һ����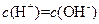
D����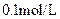 ��ˮ�м�������
��ˮ�м�������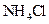 ���壬��Һ��
���壬��Һ��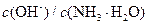 ����
����
5������� ��ҵ���õ�ⱥ��NaCl��Һ�ķ�������ȡNaOH��Cl2��H2����������Ϊԭ������һϵ�л�����Ʒ����Ϊ�ȼҵ��
��1����������Ĥ��������ʳ��ˮʱ��Cl2����NaOH��ֽӴ������²������NaClO��H2����Ĥ��������ʳ��ˮ��Ӧ�����ӷ���ʽΪ?��
��2���ȼҵ���ܸߣ�һ�ֽ�������ȼ�ϵ������ϵ��¹��տ��Խڣ��磩��30�����ϡ������ֹ�������У�������ϵĴ�����ת����ϵ����ͼ��ʾ�����еĵ缫δ��������õ�����Ĥ��ֻ����������ͨ����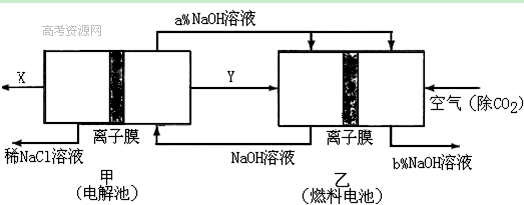
�پ����Ƶı���NaCl��ҺӦ��ͼ�е��ص�?����д���� ���ҡ�����ע�롣
��ͼ��X��____?__���ѧʽ�����������ҵĵ缫��ӦʽΪ��?_?��ͼʾ������������Һ��������a����b���Ĺ�ϵ��???������ĸ����?
A. a%=b%? B. a%��b%? C. a%��b%
�ۼ��е����ӽ���ĤΪ?��������ӽ���Ĥ���������ӽ���Ĥ������
��3���ȼҵ�IJ���NaOH�벻ͬ���ʷ�Ӧ�������ɲ�ͬ���Ρ���֪�����£�Ũ�Ⱦ�Ϊ0.1 mol/L��4��������ҺpH���±���
| ���� | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |