时间:2020-08-23 06:37:27
1、填空题 【化学―选修3 物质结构与性质】(15分)
A、B、C、D、E是原子序数逐渐增大的1-36号元素。A原子核外有4个原子轨道填充了电子;B的第一电离能比同周期相邻元素的第一电离能大,其气态氢化物在水中的溶解度在同族元素氢化物中最大;C的最高化合价和最低化合价的代数和为4;D原子的M层和N层电子数均比E原子少4个,E是人体必须的微量元素。
试根据 以上信息,回答下列问题:
以上信息,回答下列问题:
(1)A原子的电子排布图?,E原子的外围电子排布式为?。
(2)AC2分子中含有?个π键。
(3)含C50%的C的氧化物的空间构型为_________,C的原子轨道采用______杂化。
(4)写出A的常见氧化物与B的氧化物中互为等电子体的一组?。
(5)已知D的晶体在不同温度下有A、B两种堆积方式,则A、B两晶胞中D原子的配位数之比?; 晶体的密度之比为?。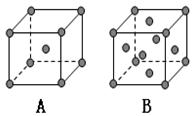
参考答案:
(1)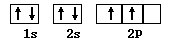 (1分)? 4S24P4 (2分)
(1分)? 4S24P4 (2分)
(2)2?(2分)?(3)V形?(2分)? SP2 (2分)
(4)CO2、N2O (2分)?(5)2 :3 (2分)?约0.92(2分)
本题解析:略
本题难度:一般
2、选择题 水的状态除了气、液和固态外,还有玻璃态,它是由液态水急速冷却到165K时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,则下列有关玻璃态水的叙述中正确的是
[? ]
A.玻璃态是水的一种特殊状态
B.水由液态变为玻璃态,体积膨胀
C.水由液态变为玻璃态,体积缩小
D.玻璃态的水是晶体
参考答案:A
本题解析:
本题难度:简单
3、填空题 [三选一―选修3:物质结构与性质]
第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物。 ?
(1)①H、C、N、O四种元素的电负性由小到大的顺序为?____________。
②下列叙述不正确的是____________。(填字母) ?
A.因为HCHO与水分子间能形成氢键,所以CH2O易溶于水 ?
B.HCHO和CO2分子中的中心原子均采用sp2杂化 ?
C.C6H6分子中含有6个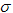 键和1个大
键和1个大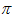 键,C2H2是非极性分子 ?
键,C2H2是非极性分子 ?
D.CO2晶体的熔点、沸点都比二氧化硅晶体的低?
③氰酸(HOCN)是一种链状分子,它与异氰酸(HNCO)互为同分异构体,其分子内各原子最外层均已达到稳定结构,试写出氰酸的结构式____________。
(2)?Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是_____________?
②六氰合亚铁离子[Fe(CN)6]4?-中不存在_______________。
A、共价键?B、非极性键?C、配位键?D、σ键?E、π键
写出一种与?CN-?互为等电子体的单质分子式______________。
(3)根据元素原子的外围电子排布特征,可将周期表分成五个区域,其中Ti属于_________?区。
(4)一种Al-Fe合金的立体晶胞如下图所示。请据此回答下列问题:?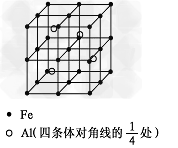
①?确定该合金的化学式__________?。
②?若晶体的密度=ρ?g/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为_______________cm。
参考答来源:91考试网 91ExAm.org案:(1)①H<C<N<O ;?②BC ;?③N≡C-O-H
(2)①具有孤对电子 ;?②B?;?N2?
(3)d区
(4)?①Fe2Al? ;②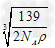
本题解析:
本题难度:一般
4、简答题 已知A、B、C、D、E都是元素周期表中前36号的元素,其原子序数依次增大.A与其他4种元素既不在同一周期又不在同一族.B和C属同一主族,D和E属同一周期,又知E是周期表中1-18列中的第8列元素.D的原子序数比E小6,D跟B可形成离子化合物其晶胞结构如图.请回答:
(1)A与B形成的化合物在固态时的晶体类型是______;A与B形成的化合物比A与C形成的化合物熔点要______(填高、低)
(2)写出C的单质与水反应的离子方程式______;
(3)如图所示,D跟B形成的离子化合物的化学式为______;鉴别该离子化合物是否为晶体,最可靠的科学方法是______,该离子化合物晶体的密度为ag?cm-3,B、D两元素的相对原子质量分别为b、c,则晶胞的体积是______cm3(只要求列出算式).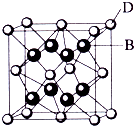
参考答案:已知A、B、C、D、E都是元素周期表中前36号的元素,其原子序数依次增大,E是周期表中1-18列中的第8列元素,所以E是Fe元素;D的原子序数比E小6,所以D是Ca元素;D跟B可形成离子化合物,该晶胞中含有B离子8个,D离子个数8×18+6×12=4,所以该化学式为D2B,B为第VIIA族元素,B和C属同一主族,且B的原子序数小于C,所以B是F元素,C是Cl元素,A与其他4种元素既不在同一周期又不在同一族,所以A是H元素.
(1)HF是共价化合物,形成的晶体是分子晶体,分子晶体的中物质的沸点随着相对分子质量的增大而增大,但分子间形成氢键的化合物使物质的沸点升高,氟化氢中含有氢键,氯化氢中不含氢键,所以氟化氢的沸点高于氯化氢,故答案为:分子晶体;高;
(2)氯气和水反应生成强电解质氯化氢和弱电解质次氯酸,所以其离子方程式为:Cl2+H2O=H++Cl-+HClO,故答案为:Cl2+H2O=H++Cl-+HClO;
(3)Ca元素跟F元素可形成离子化合物,该晶胞中含有B两离子8个,D离子个数8×18+6×12=4,所以该化学式为CaF2,鉴别该离子化合物是否为晶体,最可靠的科学方法是X射线衍射法;
每个氟化钙晶胞中含有4个钙离子、8个氟离子,所以每个晶胞的质量为4MNA,密度是ag?cm-3,所以晶胞的体积=4(c+2b)NAacm3=8b+4caNAcm3,
故答案为:CaF2;X射线衍射法;8b+4caNA.
本题解析:
本题难度:一般
5、选择题 三氯化磷分子的空间构型是三角锥形而不是平面正三角形,下列关于三氯化磷分子空间构型理由的叙述,不正确的是
[? ]
参考答案:D
本题解析:
本题难度:简单