时间:2020-08-23 05:52:57
1、选择题 微型音像磁带中磁性材料的化学组成相当于CoxFe3-xO4+x,若x的值为0.5,则下列说法中正确的是
[? ]
A、只含Co3+、Fe3+
B、含有Co3+、Fe2+、Fe3+
C、其中Co3+与Fe2+的物质的量之比为1:1
D、其中Co3+与Fe3+的物质的量之比为1:4
参考答案:A
本题解析:
本题难度:简单
2、填空题& nbsp; 现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
| A原子核外电子分占3个不同能级,且每个能级上排布的电子数相同 |
| B元素原子的核外p电子总数比s电子总数少1 |
| C原子p轨道上成对电子数等于未成对电子数,且与A同周期 |
| D元素的族序数与周期数的差为4,且不与A元素在同一周期 |
| E位于周期表中第七列 |
| F元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
参考答案:(1)4
(2)1s22s22p63s23p63d5或[Ar]3d5
(3)CH4<NH3<H2O N2O
(4)sp3 三角锥形
(5)12 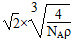
本题解析:A的电子排布式为1s22s22p2,为C元素;B的电子排布式为1s22s22p3,为N元素;C的电子排布式为1s22s22p4,为O元素;D为Cl元素,E为Mn元素,F为Cu元素。
(1)有几个电子就有几种运动状态,所以C元素的最外层应有4种不同运动状态的电子。
(3)对于CH4、NH3、H2O,由于H2O、NH3均存在分子间氢键,所以熔点H2O>NH3>CH4,在C、N、O组成的分子中与CO2互为等电子体的分子为N2O。
(4)NCl3中N原子采取sp3杂化,其分子空间构型为三角锥形。
(5)铜原子半径为面对角线的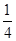 ,设棱长为a,
,设棱长为a,
则a3・ρ・NA=4×64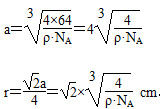
本题难度:一般
3、选择题 将元素的原子序数相加可进行有趣的金字塔堆积游戏,如图1表示丙元素的原子序数等于甲、乙两元素的原子序数之和.利用这种堆积方法,可知图1金字塔中Z元素在元素周期表中的位置为( )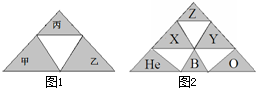
A.第三周期ⅦA族
B.第四周期ⅡA族
C.第三周期ⅠA族
D.第四周期ⅠA族
参考答案:根据题中信息:丙元素的原子序数等于甲、乙两元素的原子序数之和,可以知道X的原子序数是He和B的原子序数和,即为7,Y的原子序数是O和B的原子序数和,即为13,Z的原子序是X和Y的原子序数的和,即为20,即为Ca元素,在周期表中的位置是第四周期ⅡA族.
故选B.
本题解析:
本题难度:一般
4、选择题 关于含高能量的正离子N5+的化合物N5AsF6,下列叙述中错误的是
[? ]
A.N5+共有34个核外电子
B.N5+中氮原子间以共价键结合
C.化合物N5AsF6中As的化合价为+1价
D.化合物N5AsF6中F的化合价为 -1价
参考答案:C
本题解析:
本题难度:简单
5、选择题 下列各组分子中,中心原子均采取sp3不等性杂化的是
A.PCl3、NH3
B.BF3、H2O
C.CCl4、H2S
D.BeCl2、BF3
参考答案:A
本题解析:如果形成的杂化轨道中,如果有孤对电子就是不等性的杂化,如果没有孤对电子,全部参与成键,则是等性的,据此可知PCl3、NH3、H2O、H2S中的P、N、O、S等均是不等性杂化,答案选A。?
点评:该题是中等难度的试题,主要是考查学生对分子杂化轨道类型的熟悉了解程度,难度不大。该题的关键是明确杂化轨道的不等性含义以及判断依据,然后结合具体的化学式灵活运用即可。
本题难度:一般