时间:2020-08-13 07:17:20
1、选择题 下列说法正确的是
A.将25℃纯水加热至95℃时,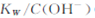 增大
增大
B.将pH=11的Na2CO3溶液加水稀释,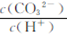 增大
增大
C.室温下,pH=a的盐酸与pH=b的氨水等体积混合后pH=7,则a+b="14"
D.0.1mol・L-酸HA与0.1mol・L-NaOH溶液等体积混合后pH>7,则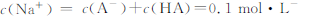
2、填空题 (8分)
Ⅰ.醋酸是常见的弱酸。用0.1 mol?L―1NaOH溶液分别滴定体积均为20.00 mL、浓度均为0.1 mol?L―1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH体积而变化的两条滴定曲线。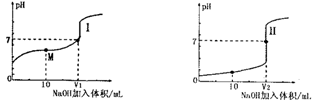
(1)滴定醋酸的曲线是 (填“I”或“Ⅱ”)。
(2)滴定开始前,三种溶液中由水电离出的c(H+)最大的溶液名称是 。
(3)V1和V2的关系:V1 V2(填“>”、“=”或“<”)
(4)M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是 。
Ⅱ.草酸钴是制备钴的氧化物的重要原料。下图为二水合草酸钴(CoC2O4?2H2O)在空气中受热的质量变化曲线,曲线中300 ℃及以上所得固体均为钴氧化物。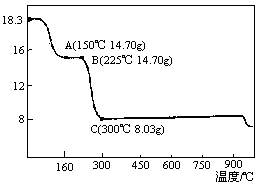
(1)通过计算确定C点剩余固体的化学成分为 (填化学式)。试写出B点对应的物质与O2在225 ℃~300 ℃发生反应的化学方程式: 。
(2)取一定质量的二水合草酸钴分解后的钴氧化物(其中Co的化合价为+2、+3),用480 mL5 mol/L盐酸恰好完全溶解固体,得到CoCl2溶液和4.48 L(标准状况)黄绿色气体。试确定该钴氧化物中Co、O的物质的量之比 。
3、选择题 25℃时,向纯水中加入NaOH,使溶液的pH=11,则由NaOH电离出的OH-离子浓度与水电离的OH-离子浓度之比为
[? ]
A. 1010:1?
B.? 5×109:1?
C. 108:1?
D. 1:1
4、选择题 下列电离方程式错误的是( ? )
A.H2CO3?2H++CO32-
B.NaHSO4(溶液)=Na++H++SO42-
C.NaHCO3=Na++HCO3-
D.CaCO3=Ca2++CO32-
5、选择题 25℃时,水的电离达到平衡:H2O  H++OH- ,下列叙述正确的是
H++OH- ,下列叙述正确的是
A. 表示的粒子不会对水的电离平衡产生影响
表示的粒子不会对水的电离平衡产生影响
B. 表示的物质加入水中,促进水的电离,c(H+)增大
表示的物质加入水中,促进水的电离,c(H+)增大
C.25℃时, 表示的微粒加入水中,促进水的电离,KW不变
表示的微粒加入水中,促进水的电离,KW不变
D.水的电离程度只与温度有关,温度越高,电离程度越大