ʱ��:2020-08-13 05:40:22
1��ѡ���� �����£���0.01 mol��L��1 Na2SO3��Һ��0.01 mol��L��1 KHSO3��Һ�������ϣ������Ի�Ϻ���Һ������ı仯���������ж���ȷ����(? )
A����Ϻ���Һ�д����й�ϵ��C(K��)��C(Na��)��C��H��)=C(SO32��)��C(HSO3��)��C��OH����
B����Ϻ���Һ�д����й�ϵ��C(K��)+C(H2SO3)+C(H��)=C(SO32��)��C��OH����
C����Ϻ���Һ�д����й�ϵ��C(SO32��)+C(HSO3��)+C(H2SO3)��0.02 mol/L
D������Һ���ǰ��Na2SO3��Һ�У�ˮ�����C��H��)С��KHSO3��Һ��ˮ�����C��H��)
�ο��𰸣�B
���������A�����ݵ���غ�ɵ�C(K��)��C(Na��)��C��H��)=2C(SO32��)��C(HSO3��)��C��OH����.����B.���ݵ���غ�ɵ�C(K��)��C(Na��)��C��H��)=2C(SO32��)��C(HSO3��)��C��OH�����������������ʵ����Ĺ�ϵ�ɵ�C(Na��) =C(SO32��)��C(HSO3��) ��C(H2SO3)�������һ��ʽ�ӣ������ɵ�C(K��)+C(H2SO3)+C(H��)=C(SO32��)��C��OH��������ȷ��C����Ϻ���Һ�е������������غ��ϵ��֪�� C(SO32��)+C(HSO3��)+C(H2SO3)����0.01+0.01����2="0.01" mol/L.����D������Һ���ǰ����Na2SO3��Һ�У�����SO32-��H2SO3����������������ӣ���KHSO3��Һ��HSO3����H2SO3һ��������������ӣ�����SO32-һ��ˮ��ˮ��̶ȴ��ڶ���HSO3����ˮ��̶ȡ�ˮ��̶�Խ��ˮ�������������Ũ��Խ���������Һ���ǰ��Na2SO3��Һ�У�ˮ�����C��H��)����KHSO3��Һ��ˮ�����C��H��)������
�����Ѷȣ�һ��
2��ѡ���� ��������pH��ֽ�ⶨij��Һ��pH�������pH��ֽ������ˮ��ʪ���ٰѴ���Һ�ε�pH��ֽ�ϣ�����ɫ�����գ����pH��6�������Һ��ʵ��pH
A������6
B����6
C������6
D������7
�ο��𰸣�B
���������pH��ֽʹ��ʱ����������ˮ��ʪ������ʪ���ᵼ����ҺŨ�Ƚ��ͣ���������Һ��˵����ʪ��PH=6��˵��ԭ��Һ��������Ũ�ȴ���PH<6��ѡB��
���㣺����PH��ֽ��ʹ�á�
�����Ѷȣ�һ��
3��ѡ����  ��һ���¶��£�HCN��ˮ�д��ڵ���ƽ�⣺HCN
��һ���¶��£�HCN��ˮ�д��ڵ���ƽ�⣺HCN H+ + CN��������˵�������
H+ + CN��������˵������� ͨ��HCl���壬Q��K��ƽ�������ƶ�
ͨ��HCl���壬Q��K��ƽ�������ƶ�
�����¶ȣ���ҺpH��С ϡ����Һ������ƽ�ⳣ����С
ϡ����Һ������ƽ�ⳣ����С
D������NaCN���壬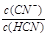 ����
����
�ο��𰸣�C
���������
�𰸣�C
A����ȷ��ͨ��HCl���壬H��Ũ������ƽ�������ƶ���
B����ȷ�����������ȷ�Ӧ�������¶ȣ�ƽ�������ƶ���H��Ũ��������ҺpH��С
C������ȷ��ϡ����Һ������ƽ�ⳣ�����䣻
D����ȷ��CN�DŨ������ķ��ȴ���HCN��
�����Ѷȣ���
4������� ��8�֣�����HA��HB��HC����һԪ���ᣬ�������ش��������⣺
�ٵ�PHֵ�������ᣬ��ˮϡ�͵�PHֵ�仯��ͼ�Ƚ������������ǿ��?��
?��??����������ʵ���Ũ���ɴ�С��˳��?��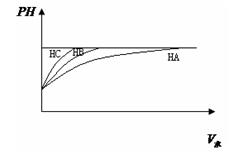
��ͬŨ�ȵ�NaA, NaB, NaC��PHֵ�Ĵ�С?��?��?��
��25��ʱ����֪NH4B����Һ�����ԣ���NH4A��Һ��PHֵ??7��д��NH4C��ˮ������ӷ���ʽ?��
��PH=2��HA��PH=12��NaOH�������Ϻ���Һ������Ũ���ɴ�С��˳����?��
�ο��𰸣���8�֣�
�� HC �� HB �� HA��1�֣�
���ʵ���Ũ���ɴ�С��˳��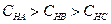 ��1�֣�
��1�֣�
��PHֵ�Ĵ�С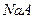 ��
��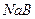 ��
��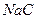 ��2�֣�
��2�֣�
��PHֵ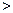 7 ��1�֣�
7 ��1�֣�
���ӷ���ʽ ��1�֣�
��1�֣�
��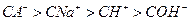 ��2�֣�
��2�֣�
�����������
�����Ѷȣ�һ��
5������� ��ȡ����п�ۣ��ֱ�ʢ�ڼס��ҡ�����֧�Թ��У�������Ҫ���������ʺ��������ӣ���ʱ�ⶨ�������������������50 mL pH��3�����ᣬ�Ҽ���50 mL pH��3�Ĵ��ᣬ������50 mL pH��3�Ĵ��ἰ����������ĩ������Ӧ���ˣ��������������һ���࣬��û��ʣ���п�����á����������������ش����и��⡣
��1����ʼʱ����Ӧ���ʵĴ�СΪ ��
��2����֧�Թ��вμӷ�Ӧ��п������Ϊ ��
��3����Ӧ���ˣ�����ʱ��Ϊ ��
��4���ڷ�Ӧ�����У��ҡ������ʲ�ͬ��������(��Ҫ˵��) ��
�ο��𰸣���1���ף��ң�������2���ף��ң�������3���ף��ң�����4������γ�ԭ��أ��ӿ��˷�Ӧ���ʡ�
�����������1����ʼʱ��������Һ��pH��ȣ�������Ũ����ȣ���Ӧ���ʵĴ�СΪ�ף��ң�������2����֧�Թ����������������һ���࣬����������п������ͭ��Ӧ���μӷ�Ӧ��п������Ϊ�ף��ң�������3�����ŷ�Ӧ�Ľ��У��Һͱ��д���ϵ��룬������Ũ�ȴ��ڼף����м����˵������γ�ԭ��أ��ʷ�Ӧ���ʣ��ף��ң���������ʱ��Ϊ�ף��ң�������4���ڷ�Ӧ�����У��ҡ������ʲ�ͬ������������γ�ԭ��أ��ӿ��˷�Ӧ���ʡ�
���㣺����ǿ������ʵĶԱȡ�Ӱ�췴Ӧ���ʵ����ء�
�����Ѷȣ�һ��