时间:2020-08-13 05:40:22
1、选择题 常温下,将0.01 mol・L-1 Na2SO3溶液与0.01 mol・L-1 KHSO3溶液等体积混合,若忽略混合后溶液的体积的变化,则下列判断正确的量(? )
A.混合后溶液中存在有关系:C(K+)+C(Na+)+C(H+)=C(SO32-)+C(HSO3-)+C(OH-)
B.混合后溶液中存在有关系:C(K+)+C(H2SO3)+C(H+)=C(SO32-)+C(OH-)
C.混合后溶液中存在有关系:C(SO32-)+C(HSO3-)+C(H2SO3)=0.02 mol/L
D.两溶液混合前,Na2SO3溶液中,水电离出C(H+)小于KHSO3溶液中水电离出C(H+)
2、选择题 常温下用pH试纸测定某溶液的pH,如果将pH试纸用蒸馏水润湿后,再把待测液滴到pH试纸上,跟比色卡对照,测得pH=6。则此溶液的实际pH
A.大于6
B.小于6
C.等于6
D.大于7
3、选择题  在一定温度下,HCN在水中存在电离平衡:HCN
在一定温度下,HCN在水中存在电离平衡:HCN H+ + CN-。下列说法错误的
H+ + CN-。下列说法错误的 通入HCl气体,Q>K,平衡逆向移动
通入HCl气体,Q>K,平衡逆向移动
升高温度,溶液pH减小 稀释溶液,电离平衡常数减小
稀释溶液,电离平衡常数减小
D.加入NaCN固体,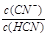 增大
增大
4、填空题 (8分)现有HA、HB、HC三种一元弱酸,分析并回答下列问题:
①等PH值的三种酸,加水稀释的PH值变化如图比较三种酸的酸性强弱?〉
?〉??三种酸的物质的量浓度由大到小的顺序?。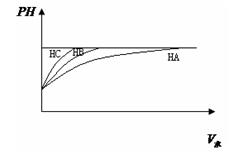
②同浓度的NaA, NaB, NaC,PH值的大小?〉?〉?。
③25℃时若已知NH4B的溶液显中性,则NH4A溶液的PH值??7,写出NH4C的水解的离子方程式?。
④PH=2的HA与PH=12的NaOH等体积混合后,溶液中离子浓度由大到小的顺序是?。
5、填空题 称取三份锌粉,分别盛于甲、乙、丙三支试管中,按下列要求另加物质后,塞上塞子,定时测定生成氢气的体积。甲加入50 mL pH=3的盐酸,乙加入50 mL pH=3的醋酸,丙加入50 mL pH=3的醋酸及少量胆矾粉末。若反应终了,生成氢气的体积一样多,且没有剩余的锌。请用“>”“=”或“<”回答下列各题。
(1)开始时,反应速率的大小为 。
(2)三支试管中参加反应的锌的质量为 。
(3)反应终了,所需时间为 。
(4)在反应过程中,乙、丙速率不同的理由是(简要说明) 。