时间:2020-08-13 05:40:22
1、选择题 当NaOH溶液与氨水的pH、体积都相同时,下列叙述正确的是
[? ]
A.两溶液的物质的量浓度相同
B.两溶液的c(H+)相同
C.用同浓度盐酸中和时,消耗酸的体积相同
D.升高温度10℃,两者pH仍相等
参考答案:B
本题解析:
本题难度:一般
2、选择题 下列物质中能抑制水的电离且使溶液呈现出酸性的是( )
A.Na2CO3
B.Al2(SO4)3
C.K2SO4
D.H2SO4
参考答案:D
本题解析:
本题难度:一般
3、简答题 (16分)资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体并生成白色不溶物
(1)提出假设
猜想①:白色不溶物可能为___
猜想②:白色不溶物可能为MgCO3
猜想③:白色不溶物可能是碱式碳酸镁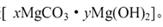
(2)定性实验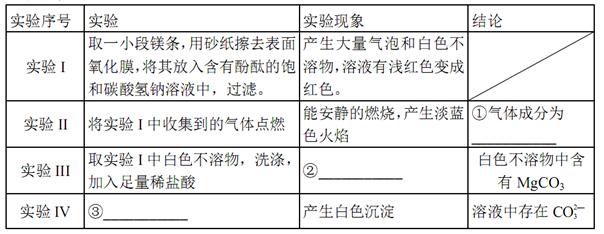
(3)定量实验:
称取实验I中所得干燥、纯净的白色不溶物14.2 g,充分加热至不在产生气体为止,并使分解
产生的气体全部通入如下装置中: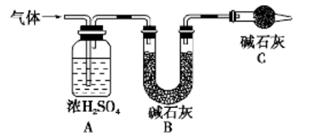
①实验测得装置A增重1.8 g,装置B增重4.4 g,则白色不溶物的化学式为_____
②装置C的作用为____,若移除装置C会导致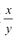 的值___(填“偏大”、“偏小”或“不变”
的值___(填“偏大”、“偏小”或“不变”
(4)探究原理
①请结合化学用语和化学平衡移动原理解释Mg与饱和NaHC03溶液反应产生大量气泡和白
色不溶物的原因:_______
②250C时,测得Mg与饱和NaHC03溶液反应所得混合体系的pH为10,则该体系中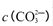
为(已知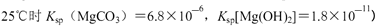
参考答案:(16分)
(1)Mg(OH)2(1分)
(2)①氢气(1分)?②沉淀溶解,产生气泡(2分)
③取实验I中的澄清溶液少许于试管中,加入少量CaCl2溶液(2分)
(3)①MgCO3?Mg(OH)2[或Mg(OH)2?MgCO3或Mg2(OH)2CO3](2分)
②防止空气中的水蒸气和二氧化碳进入装置B引起实验误差(2分)
偏大(1分)
(4)①NaHCO3溶液中存在平衡:HCO3?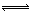 H++CO32?;H2O
H++CO32?;H2O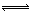 H++OH?,Mg和H+反应生成H2和Mg2+,使上述两平衡向右移动,c(CO32?)、c(OH?)均增大,Mg2+跟OH?、CO32?反应生成难溶物Mg(OH)2?MgCO3(3分)
H++OH?,Mg和H+反应生成H2和Mg2+,使上述两平衡向右移动,c(CO32?)、c(OH?)均增大,Mg2+跟OH?、CO32?反应生成难溶物Mg(OH)2?MgCO3(3分)
② 3.8×10-3mol?L?1(2分)
本题解析:(1)对比猜想②③,可知猜想①白色不溶物可能为Mg(OH)2.
(2)①气体能安静的燃烧,产生淡蓝色火焰,所以该气体为H2。
②结论为白色不溶物中含有MgCO3,所以加入足量稀盐酸,实验现象为:沉淀溶解,产生气泡。
③证明溶液中含有CO32?,所以现象为产生白色沉淀,所以实验操作为:取实验I中的澄清溶液少许于试管中,加入少量CaCl2溶液。
(3)①装置A增重1.8 g,生成了H2O为0.1mol,装置B增重4.4 g,生成CO2的物质的量为0.1mol,则白色不容物含有等物质的量的Mg(OH)2和MgCO3,所以白色不溶物的化学式为:MgCO3?Mg(OH)2[或Mg(OH)2?MgCO3或Mg2(OH)2CO3]
②装置C中含有碱石灰,能吸收水分和CO2,所以其作用为防止空气中的水蒸气和二氧化碳进入装置B引起实验误差;若移除装置C外界,空气中的水蒸气和二氧化碳进入装置B,而装置B增加的质量为产生的CO2的质量,所以造成测量的MgCO3的质量增大,导致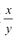 的值偏大。
的值偏大。
(4)①NaHCO3溶液中存在两个电离平衡:HCO3?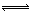 H++CO32?;H2O
H++CO32?;H2O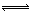 H++OH?,加入Mg后,Mg和H+反应生成H2和Mg2+,使上述两平衡向右移动,c(CO32?)、c(OH?)均增大,Mg2+跟OH?、CO32?反应生成难溶物Mg(OH)2?MgCO3。
H++OH?,加入Mg后,Mg和H+反应生成H2和Mg2+,使上述两平衡向右移动,c(CO32?)、c(OH?)均增大,Mg2+跟OH?、CO32?反应生成难溶物Mg(OH)2?MgCO3。
②pH为10,则c(OH?)=10-4mol?L?1,c(Mg2+)=Ksp[Mg(OH)2]÷c2(OH?)=1.8×10-11÷(10-4)2=1.8×10-3,c(CO32?)=" K" sp[MgCO3]÷c(Mg2+)=6.8×10-6÷(1.8×10-3)= 3.8×10-3mol?L?1sp的计算。
本题难度:一般
4、填空题 NaHCO3在水溶液中,HCO3-的电离程度小于HCO3-的水解程度。回答下列有关问题:
⑴H2CO3的电离方程式为?;
⑵NaHCO3溶液显碱性,原因是(用离子方程式表示)
?;
⑶在该溶液中,c(Na+)、c(H+)、c(HCO3-)、c(OH-)的大小关系为
?;
⑷根据电荷守恒原理,该溶液中离子浓度关系有:
c(Na+)+c(H+)=?;
⑸根据物料守恒原理,该溶液中离子浓度关系有:
c(Na+)=?。
参考答案:⑴H2CO3? H++HCO3-,? HCO3-? H++CO32-; ⑵HCO3-+H2O? H2CO3+OH-;?⑶c(Na+)>c(HCO3-)>c(OH-)>c(H+);
⑵HCO3-+H2O? H2CO3+OH-;?⑶c(Na+)>c(HCO3-)>c(OH-)>c(H+);
⑷c(HCO3-)+c(OH-)+2c(CO32-);?⑸c(HCO3-)+c(H2CO3)+c(CO32-)(各1分)
本题解析:略
本题难度:简单
5、选择题 用水稀释0.1 mol・L-1氨水时,溶液中随水量的增加而减小的是? ( )。
A.c(OH-)/c(NH3・H2O)
B.c(NH3・H2O)/c(OH-)
C.n(OH-)和c(H+)
D.c(H+)和c(OH-)的乘积
参考答案:B
本题解析:加水促进NH3・H2O的电离,使n(NH3・H2O)减小,n(OH-)增大,c(OH-)减小,但c(H+)和c(OH-)的乘积即KW不变,则c(H+)增大。因此c(NH3・H2O)/c(OH-)=n(NH3・H2O)/n(OH-)减小。
本题难度:简单