时间:2019-05-30 04:24:12
1、选择题 将0.1 mol·L-1 CH3COOH溶液加水稀释或加入少量的CH3COONa晶体时,都会引起
[? ]
A.溶液的pH增加
B.溶液中的c(H+)增大
C.溶液的导电能力减弱
D.溶液中的c(OH-)减小
参考答案:A
本题解析:
本题难度:一般
2、选择题 室温下,有pH=3的盐酸、硫酸、醋酸(假设HAc的电离度为1%)三种相同体积的溶液。以下叙述错误的是
A.测定其导电性能相同
B.与足量的锌粉反应的起始速率相同
C.与足量的锌粉反应产生氢气的体积比为1∶1∶100
D.与同浓度氢氧化钠溶液反应,消耗氢氧化钠溶液的体积为1∶2∶100
参考答案:D
本题解析:A、pH=3的盐酸、硫酸、醋酸导电性能相同,正确;B、pH=3的盐酸、硫酸、醋酸,锌与氢离子反应,氢离子浓度相同,起始速率相同,正确;C、HAc的电离度为1%,PH="3" ,与足量的锌粉反应,HAc均被消耗,CHAc=10-3/1%=10-1,盐酸和硫酸的浓度与氢离子浓度相等,10-3, 足量的锌粉反应产生氢气的体积比为1∶1∶100,正确;D、,消耗氢氧化钠溶液的体积为1∶1∶100,错误。
本题难度:一般
3、选择题 pH相同的CH3COOH和HCl溶液,分别用蒸馏水稀释至原体积的m倍和n倍,稀释后两溶液的pH仍然相同,则m和n的关系是
A.m<n
B.m>n
C.m=n
D.不能确定
参考答案:B
本题解析:HCl是强酸,而CH3COOH是弱酸,存在电离平衡,稀释过程促进CH3COOH电离,向生成H+ 的方向移动,稀释前两溶液的pH相同,即c(H+)相同,若要稀释后两溶液的pH仍然相同,在CH3COOH溶液中要加入更多的水,才能保持CH3COOH和HCl溶液的pH仍然相同。选B。
本题难度:一般
4、选择题 常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000倍,其pH与所加水的体积变化如图所示,则下列结论中正确的是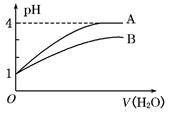
A.A酸比B酸的电离程度小
B.B酸比A酸容易电离
C.A是强碱,B是弱碱
D.pH=1时,B酸的物质的量浓度比A酸大
参考答案:D
本题解析:本题难易程度为中等,根据酸溶液稀释pH变化规律,强酸溶液:pH=a,加水稀释10n倍,则pH=a+n弱酸溶液:pH=a,,加水稀释10n倍,则a<pH<a+n。酸溶液的pH不可能大于7可知A酸为强酸,B为弱酸。所以C选项错误。
A选项错误,强酸为强电解质完全电离,弱酸部分电离。所以A酸比B酸的电离程度大。
B选项错误,强酸比弱酸容易电离。A酸比B酸容易电离.
D选项正确,pH相同时,弱酸的物质的量浓度比强酸大。
本题难度:一般
5、选择题 部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | K=1.77×10-4 | K=4.9×10-10 | K1=4.2×10-7 K2=5.6×10-11 |
参考答案:A
本题解析:根据表中数据判断酸性强弱顺序为:HCOOH >H2CO3>HCN >HCO3-,结合强酸制弱酸的原理分析,A正确;B、酸性:HCOOH >HCN,根据水解理论,碱性:HCOONa<NaCN;C、酸的物质的量相同,消耗氢氧化钠一样多;D、NaHCO3溶液呈碱性,水解程度大于电离程度。
本题难度:一般