时间:2019-03-14 22:37:34
1、填空题 (1)氯化铝水溶液呈 性(填“酸性”,“中性”或“碱性”),原因是(用离子方程式表示): 。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是(写化学式) 。实验室在保存AlCl3溶液时,常在溶液中加少量的 ,以 (填“促进”、“抑制”)其水解。
(2)将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈 性(填“酸性”,“中性”或“碱性”),溶液中c(Na+) c(CH3COO-)(填“ >” 或“=”或“<”)。
(3)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈 性,(填“酸性”,“中性”或“碱性”)溶液中c(Na+) c(CH3COO-) (填“ >” 或“=”或“<”)。
(4) 物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中醋酸根离子和钠离子浓度相等,则混合后溶液呈 性,(填“酸性”,“中性”或“碱性”),醋酸体积 氢氧化钠溶液体积(填“ >” 或“=”或“<”)。
(5)已知0.1 mol・L-1的NaHCO3溶液PH=9,则溶液中c(CO32-) c(OH-) (填“ >” 或“=”或“<”),其溶液显电中性的原因 (用离子浓度关系式表示)。
参考答案:(1)酸,AI3++3H2O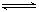 AI(OH)3+3H+ AI2O3 HCI 抑制
AI(OH)3+3H+ AI2O3 HCI 抑制
(2)碱, c(Na+)>c(CH3COO-)。(3)酸, c(Na+)<c(CH3COO-) 。
(4)中,>。(5)c(CO32-)<c(OH-),2c(CO32-)+c(OH-)+c(HCO3-)=c(Na+)+c(H+)
本题解析:(1)氯化铝是强酸弱碱盐,水解显酸性,方程式是AI3++3H2O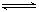 AI(OH)3+3H+。水解是吸热的,加热促进水解,且生成的氯化氢挥发,所以最终生成的是氢氧化铝,灼烧则得到氧化铝。所以实验室在保存AlCl3溶液时,常在溶液中加少量的盐酸,以抑制氯化铝的水解。
AI(OH)3+3H+。水解是吸热的,加热促进水解,且生成的氯化氢挥发,所以最终生成的是氢氧化铝,灼烧则得到氧化铝。所以实验室在保存AlCl3溶液时,常在溶液中加少量的盐酸,以抑制氯化铝的水解。
(2)醋酸和氢氧化钠的物质的量相等,恰好反应,生成醋酸钠。醋酸钠水解,溶液显碱性。所以根据电荷守恒定律可知,c(Na+)>c(CH3COO-)。
(3)由于醋酸是弱酸,所以pH=3的醋酸的浓度大于0.001mol/L,则在和氢氧化钠反应时,醋酸是过量的,所以溶液显酸性。所以根据电荷守恒定律可知,c(Na+)<c(CH3COO-)。
(4)根据电荷守恒定律可知,当溶液中醋酸根离子和钠离子浓度相等是,氢离子浓度等于OH-浓度,溶液显中性。这说明醋酸应该是过量的,所以醋酸的体积大于氢氧化钠溶液的体积。
(5)0.1 mol・L-1的NaHCO3溶液PH=9,这说明碳酸氢钠的水解程度大于碳酸氢钠的电离程度,所以溶液中c(CO32-)<c(OH-)。根据电荷守恒定律可知,离子浓度的关系是2c(CO32-)+c(OH-)+c(HCO3-)=c(Na+)+c(H+)。
本题难度:一般
2、选择题 常温下,下列溶液中的离子浓度关系正确的是
A.pH =3的醋酸溶液中:c(H+)=c(CH3COO-)=3.0mol?L-1
B.Na2S溶液中:c(Na+)>c(HS-)>c(OH-)>c(H2S)
C.pH =2的盐酸与pH =12的氨水等体积混合,所得溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
D.pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③
参考答案:D
本题解析:醋酸是弱酸,部分电离,根据电荷守恒,溶液中c(H+)=c(CH3COO-)+c(OH-),A项错误;硫化钠是强电解质,电离出Na+和S2-,硫离子水解生成HS-,则溶液中离子浓度的大小关系为c(Na+)>c(OH-)>c(HS-)>c(H2S),B项错误;氨水是弱碱,pH =2的盐酸与pH =12的氨水等体积混合,溶液为氯化铵和氨水,溶液显碱性,C项错误;根据越弱越水解,酸性强弱的顺序为CH3COOH>H2CO3 >HClO,NaClO的水解能力最强,其次为NaHCO3,水解能力最弱的是CH3COONa ,则pH相同的①CH3COONa②NaHCO3③NaClO三种溶液的c(Na+):①>②>③,D项正确;选D。
考点:考查离子浓度的大小关系。
本题难度:困难
3、选择题 0.1mol・L¯1 的Na2S溶液中,下面说法正确的是
A.c(Na+) +c(H+)=c(OH-)+c(HS-)+c(S2-)
B.c(Na+) =2c(HS-) +2c(S2-) +c(H2S)
C.c(Na+)>c(OH-)>c(HS-)>c(H+)
D.c(H2S)+ c(HS-)+ c(H+)= c(OH-)
参考答案:C
本题解析:A是电荷守恒,应该为:c(Na+) +c(H+)=c(OH-)+c(HS-)+2c(S2-) ,A错,B是物料守恒,应该是 c(Na+) =c(HS-) +c(S2-) +c(H2S),B错;S2-发生水解S2- +H2O HS-+ OH-,水还会电离出OH-,故c(OH-)>c(HS-),C对;D是质子守恒,应该是2c(H2S)+ c(HS-)+ c(H+)= c(OH-),D错。选C
HS-+ OH-,水还会电离出OH-,故c(OH-)>c(HS-),C对;D是质子守恒,应该是2c(H2S)+ c(HS-)+ c(H+)= c(OH-),D错。选C
考点:盐类水解、离子浓度的大小比较。
本题难度:一般
4、选择题 下列过程或现象与盐类水解无关的是
[? ]
A. 热的纯碱液用于去油污
B. 加热氯化铁溶液颜色变深
C. 饱和食盐水使甲基橙显黄色
D. 泡沫灭火器中的Al2(SO4)3溶液不能装在铁筒里
参考答案:C
本题解析:
本题难度:简单
5、选择题 NH4Cl稀溶液中分别加入少量下列物质或改变如下条件,能使比值c(NH4+)/c(Cl―)一定增大的是
①HCl气体 ②氨气 ③H2O ④NH4Cl固体 ⑤NaOH固体 ⑥降温
A.③④⑤
B.②④
C.②③⑥
D.②④⑥
参考答案:D
本题解析:氯化铵中存在水解平衡,NH4Cl+H2O NH3・H2O+HCl。通入氯化氢,则抑制水解,但比值是减小的;通入氨气,抑制水解,比值增大;稀释促进水解,比值减小;加入氯化铵固体,抑制水解,比值增大;氢氧化钠固体促进水解,比值减小;水解吸热,降低温度,抑制水解,比值增大,因此正确的答案选D。
NH3・H2O+HCl。通入氯化氢,则抑制水解,但比值是减小的;通入氨气,抑制水解,比值增大;稀释促进水解,比值减小;加入氯化铵固体,抑制水解,比值增大;氢氧化钠固体促进水解,比值减小;水解吸热,降低温度,抑制水解,比值增大,因此正确的答案选D。
本题难度:一般