时间:2018-03-17 06:14:56
1、选择题 下列说法正确的是
[? ]
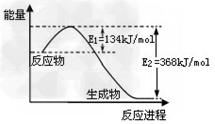
A.?已知1?mol?NO2和1?mol?CO反应生成CO2和NO过程中能量变化如图,则NO2和CO反应的热化学方程式为:NO2(g)+CO(g)=CO2(g)+NO(g);△H=?+234kJ/mol ?
B.?一定温度下,利用pH计测定不同浓度醋酸溶液的pH 值,得到数据(如上表)
当醋酸浓度为0.1mol/L时,通过计算求得该温度下醋酸的电离度为1%
C.?已知CaCO3的Ksp=2.8×10-9,现将等体积的Na2CO3溶液与CaBr2溶液混合,若CaBr2溶液的浓度为?5.6×10-5?mol/L,则生成沉淀所需Na2CO3溶液的最小浓度为?5×10-5mol/L
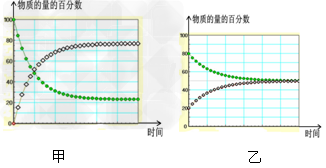
D.?在不同条件下进行的异构化反应?X Y?的进程图解。图中的“
Y?的进程图解。图中的“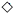 ”是X,“
”是X,“ ”是Y 则可以计算得到乙的平衡常数K=1,且比甲的平衡常数要小
”是Y 则可以计算得到乙的平衡常数K=1,且比甲的平衡常数要小
2、选择题 pH相同的醋酸和盐酸,分别用水稀释至原体积的m倍和n倍,稀释后两溶液pH仍相等,则m和n的关系是
A.m=n
B.m>n
C.m<n
D.无法比较
3、选择题 将 4 mol A 气体和 2 mol B 气体在 2 L 的容器中混合并在一定条件下发生如下反应:2A(g)+B(g) 2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol・L-1 ,现有下列几种说法中正确的是
2C(g)若经 2 s(秒)后测得 C 的浓度为 0.6 mol・L-1 ,现有下列几种说法中正确的是
①用物质A 表示的反应的平均速率为0.3 mol・L-1・S-1
②用物质B 表示的反应的平均速率为0.6 mol・L-1・S-1
③2 s 时物质A 的转化率为70%
④2 s 时物质B 的浓度为0.7 mol・L-1,
A.①③
B.①④
C.②③
D.③④
4、选择题 已知醋酸、醋酸根离子在溶液中存在下列平衡及其对应的平衡常数
CH3COOH CH3COO― + H+?K1=1.75×10-5?△H1>0
CH3COO― + H+?K1=1.75×10-5?△H1>0
CH3COO― + H2O CH3COOH + OH―?K2=5.71×10-10?△H2>0
CH3COOH + OH―?K2=5.71×10-10?△H2>0
常温下,将等体积、等物质的量浓度的醋酸和醋酸钠溶液混合,下列叙述正确的是
A.对混合溶液进行微热,K1增大、K2减小
B.混合溶液的pH<7
C.混合溶液中c(CH3COO―)>c(Na+)
D.温度不变,若在混合溶液中加入少量NaOH固体,c(CH3COO―)减小
5、填空题 (14分)下列物质中,①NaCl;②NaOH;③NH3・H2O;④CH3COOH溶液;⑤BaSO4;⑥H2O;⑦HCl;⑧H2SO4?⑨CO2;⑩酒精溶液(均填写编号回答)
⑴是弱电解质的有?,是非电解质的有?。
⑵pH相等的②的溶液和③的溶液等体积加水稀释相同倍数后,pH大的是?。
⑶有pH均为2的④、⑦、⑧三种物质的溶液,物质的量浓度大到小的顺序为?,若分别用这三种酸中和含等物质的量NaOH的溶液,所需酸溶液的体积分别为a、b、c,则a、b、c的大小关系是?。
(4)某温度时,0.01 mol?L-1的醋酸溶液电离平衡常数为1. 0×10 -8,醋酸的电离平衡常数表达式为?,达平衡时,溶液中氢离子浓度是??,当向该溶液中加入一定量的盐酸时,电离常数?发生变化(填是、否)。
(5)将pH=1的盐酸平均分成2份,1份加适量水,另1份加入与该盐酸物质的量浓度相同的适量NaOH溶液后,pH都升高了1,则加入了水与NaOH溶液的体积比为?。