ʱ��:2017-11-11 02:48:41
1������� ��100mL?FeI2��Һ����ͨ��Cl2������������Cl-��I2��Fe3+��IO3-������Fe3+��I2�����ʵ�����n��Cl2���ı仯��ͼ��ʾ����ش��������⣺
��1����ͼ��֪��I-��Fe2+��I2�������ӵĻ�ԭ����ǿ������
˳��Ϊ______��______��______��
��2����n��Cl2��=0.12molʱ����Һ�е�������ҪΪ______���ӿ�ʼͨ��Cl2��n��Cl2��=0.12molʱ���ܷ�Ӧ�Ļ�ѧ����ʽΪ______��
��3������Һ��n��Cl-����n��IO3-��=8��1ʱ��ͨ���Cl2�ڱ�״���µ����Ϊ______��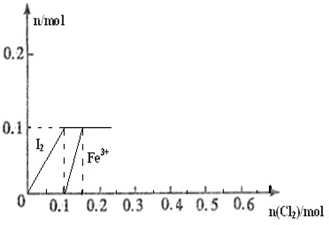
�ο��𰸣���1����100mL?FeI2��Һ����ͨ��Cl2������������Cl-��I2��Fe3+��IO3-����������ԭ��Ӧ�л�ԭ��Խǿ����Խ��Һʧ���ӣ��ɴ�˵��I-��Fe2+��I2�������ӵĻ�ԭ����ǿ������˳��ΪI-��Fe2+��I2���ʴ�Ϊ��I-��Fe2+��I2��
��2������ͼ��Ϸ�ӦCl2+FeI2=FeCl2+I2 ֪����ͨ��0.1molCl2ʱ��������ȫ���������ɵⵥ�ʣ��⻯���������ʵ�����0.1mol����100mL?FeI2��Һ����ͨ��Cl2������������Cl-��I2��Fe3+��IO3-�����Ե�ͨ��Cl2��n��Cl2��=0.12molʱ���������������ӷ�Ӧ���������ӣ�2Fe2++Cl2=2Fe3++2Cl-��ͨ�����������ʵ�����0.02molʱ����0.04mol�������ӱ���������ʣ0.06mol�������ӣ�������Һ�д��ڵ�������Fe2+��Fe3+��Cl-�����������ӷ�Ӧ����ʽΪ5FeI2+6Cl2=5I2��+2FeCl3+3FeCl2��
�ʴ�Ϊ��Fe2+��Fe3+��Cl-��5FeI2+6Cl2=5I2��+2FeCl3+3FeCl2��
��3����������ת��Ϊ���������ʱ������������ȫת��Ϊ�����ӣ������������ʵ�����x���������ӵ����ʵ�����8x������������ԭ��Ӧ�е�ʧ��������ȵ�x��6+��0.2-x����1+0.1��1=8x��1��x=0.1��������Һ�е���������ʵ�����0.1mol�������ӵ����ʵ�����0.8mol������Cl2��2Cl-֪�����������ʵ�����0.4mol�����������=0.4mol��22.4L/mol=8.96L��
�ʴ�Ϊ��8.96L��
���������
�����Ѷȣ�һ��
2��ѡ���� ��Ӧ3NO2+H2O=2HNO3+NO�У��������������뱻��ԭ�����ʵ����ʵ���֮��Ϊ��������
A��1��1
B��1��2
C��2��1
D��3��1
�ο��𰸣�C
���������
�����Ѷȣ���
3��ѡ���� ��ҵ�����÷�Ӧ��3Cl2��2NH3��N2��6HCl?��������ܵ��Ƿ�©��������˵���������
A.�÷�Ӧ���ڸ��ֽⷴӦ
B.�÷�Ӧ��Cl2��������
C.���ܵ�©�������ͻ��������
D.�÷�Ӧ����1molN2����6mol���ӷ���ת��
�ο��𰸣�A
���������
�𰸣�A
A������ȷ�������û���Ӧ��������ԭ��Ӧ��B����ȷ��Cl���ϼ۽��ͣ�C��ȷ��HCl��NH3=NH4Cl�����ǰ�ɫ���壻D����ȷ��N��-3�۱�Ϊ0�ۣ�����1molN2����6mol���ӷ���ת�ơ�
�����Ѷȣ���
4������� ������ˮ����ˮ����Ի�����ɵ���ȾԽ��Խ���أ�����ר����Ϊ�����ý�������ˮ���е�NO3-��ԭΪN2���Ӷ�������Ⱦ��
�䷴Ӧ�����ӷ���ʽ�ǣ�6NO3-+2zAl+2һH2O��3N2��+2zAl��OH��3+6OH-
��2������Ҫ��ȥ2x3����Ԫ��z.3xol�ķ�ˮ�е�NO3-���赪Ԫ�ض���NO3-����ʽ���ڣ���ͬ������������Ҫ���Ľ�����______g��
��2��������Ϊ����þ�����ܸ�������������Ⱦ���䷴Ӧԭ���ͽ�������ͬ��
��д��þ�ͺ�����ˮ��Ӧ�����ӷ���ʽ______��
����֪����þ�ǴӺ�ˮ����ȡ��xgCl2��ͨ������Ƶõģ���Ҫ��ȥ2x3����Ԫ��z.3xol�ķ�ˮ�е�NO3-����������Ҫ��z.n%������������xgCl2�ĺ�ˮ______kg��
�ο��𰸣���v����Ϊ������.3mo��e��ˮ��eNO3-e����e��Ϊ��.3mo�ң����ݻ�ѧ����ʽ6NO3-+v��A��+v8H2O�T3N2��+v��A�ң�OH��3+6OH-����.3mo��e������������Ľ�����e����e��Ϊ��.3mo�ҡ�v��6=��.5mo�ң�������Ҫ������e�����ǣ���.5mo�ҡ�27g/mo��=v3.5g��
�ʴ�Ϊ��v3.5��
��2���ٽ���þ�����ܸ���������e��Ⱦ����Ӧԭ���ͽ�������ͬ�����Բ���Ϊ������������þ�����������ӣ�
��Ӧ���ӷ���ʽΪ2NO3-+5Mg+6H2O�TN2��+5Mg��OH��2+2OH-��
�ʴ�Ϊ��2NO3-+5Mg+6H2O�TN2��+5Mg��OH��2+2OH-��
����������Ҫ����.5%������������MgC��2e��ˮmkg����
5MgC��2��������5Mg��������2NO3-
5��ͼ5g&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp; 2mo��
m��v��3g����.5%&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp;&n��sp; ��.3mo��
����5��ͼ5gm��v��3g����.5%=2mo��&n��sp;��.3mo�ң����m=v4.25��
�ʴ�Ϊ��v4.25��
���������
�����Ѷȣ�һ��
5�������� ��0.3mol NaCl������0.1mol CuSO4��5H2O����������ˮ�����1�����Һ��Ȼ��ȡ��200ml��Һ����ʯī�缫��ͨ��һ��ʱ�䣨������ˮ�⣩����Cl-����ȫ����Ϊ�����ݳ�ʱ�������ϲ����������������״���£��Ƕ��٣�������Һ��PHΪ���٣�������Һ������䣩��
�ο��𰸣�H2Ϊ0.224L��pH=13
���������
�����Ѷȣ�һ��