时间:2017-11-05 23:48:32
1、选择题 在铁与铜的混合物中,加入一定量的稀硝酸,充分反应后剩余金属m1g,再向其中加入一定量的稀硫酸,充分振荡后,剩余金属m2g,m1与m2的关系是(?)
A.m1一定大于m2
B.m1可能等于m2
C.m1一定等于m2
D.m1可能大于m2
参考答案:A
本题解析:铜和铁的化合物与硝酸反应生成硝酸盐,向硝酸盐中加入酸,相当于加硝酸,所以金属继续溶解,则m1一定大于m2。答案选A。
点评:NO3-与H+共存时,具有强氧化性。
本题难度:一般
2、填空题 固体化合物A,按下图所示发生系列变化,已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色。
(1)写出下列物质的化学式:
A:__________,B:__________,D:__________,E:__________,X:__________。
(2)写出反应①的化学方程式:________________________________。
写出反应③的离子方程式: ________________________________。
写出反应④过程中,白色沉淀在空气中久置的化学方程式:________________。
参考答案:(1)A: Fe(OH)3? B:Fe2O3 ?D:FeCl3 ?E :FeCl2? X : Fe
(2)2Fe(OH)3=Fe2O3 +3H2O;? 2Fe3++Fe=3Fe2+;? 4Fe(OH)3+O2+2H2O=4Fe(OH)3
本题解析:由图示结合“E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色”。确定A: Fe(OH)3? B:Fe2O3 ?D:FeCl3 ?E :FeCl2? X : Fe,进而解题。
本题难度:一般
3、填空题 某不锈钢(主要成分为Fe)样品中含有铝、铜等(其它成分忽略),为了测定该合金中铁的含量,有人设计如下工艺流程: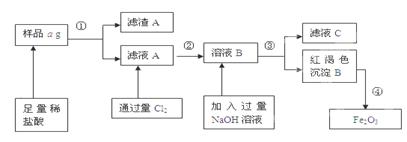
(1)滤液C中溶质含有_? _(写化学式);
(2)如何验证滤液A中含Fe2+,而不含Fe3+____?_____。
(3)对所得Fe2O3固体称量得质量为b g,计算该样品中铁元素质量分数的表达式为(用含a、b的式子表示)___?__。
参考答案:(1)NaAlO2、NaCl、NaOH (2)取少量滤液A于试管中,滴几滴KSCN溶液,溶液不变色,再加氯水(或通氯气),溶液变为血红色。 (3)(7b/10a)×100%
本题解析:(1)样品中加入足量的稀盐酸发生的反应为Fe + 2HCl=FeCl2 + H2↑;2Al+6HCl=2AlCl3+3H2↑滤液中含有FeCl2和AlCl3,滤渣中含有Cu等难溶性杂质。向滤液中通入过量的氯气发生反应2FeCl2+Cl2="=" 2FeCl3,再向溶液中加入过量的NaOH溶液时发生反应AlCl3+4NaOH=3NaCl+NaAlO2+2H2O. FeCl3+3NaOH =3NaCl+Fe(OH)3↓.过滤得到的滤液C中含有NaCl、NaAlO2、NaOH。红褐色沉淀为Fe(OH)3。将其灼烧分解得到Fe2O3和水。(2)验证滤液A中含Fe2+,而不含Fe3+的方法是取少量滤液A于试管中,滴几滴KSCN溶液,溶液不变色,再加氯水(或通氯气),溶液变为血红色。或加入氢氧化钠溶液首先产生白色沉淀。白色沉淀迅速变为灰绿色,最后变为红褐色。(3)n(Fe2O3)=bg÷160g/mol.n(Fe)=2×n(Fe2O3)=b/80mol.所以该样品中铁元素质量分数为(b/80mol×56g/mol)÷ag×100%="(7b/10a)×100%" .?3+的检验等知识。
本题难度:一般
4、选择题 取少量MgO、A12O3、SiO2、Fe2O3的混合粉末,加入过量盐酸,充分反应后过滤,得到沉淀X和滤液Y。下列叙述正确的是
[? ]
A.上述四种氧化物对应的水化物中,Al(OH)3酸性最强
B.向沉淀X中逐滴加入硝酸,沉淀慢慢溶解
C.溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+
D.溶液Y中加入过量氨水,所得沉淀为Fe(OH)3和Mg(OH)2
参考答案:C
本题解析:
本题难度:简单
5、计算题 现有表面覆盖铁锈的铁块58.16 g,与足量稀H2SO4反应,可放出22.4 L(标准状况下)H2。反应后溶液中加入KSCN溶液不显红色。求原铁块被氧化的铁的质量。
参考答案:1.12 g
本题解析:Fe+H2SO4====FeSO4+H2↑
56 g? 1 mol
Fe2O3+3H2SO4====Fe2(SO4)3+3H2O
X? x
Fe2(SO4)3+Fe====2FeSO4
X? y
x="y=0.01" mol
4Fe+3O2====2Fe2O3
0.02 mol? 0.01 mol
被氧化的铁的质量m(Fe)="0.02" mol×56 g・mol-1="1.12" g
本题难度:简单