ʱ��:2017-09-25 16:35:25
1������� �����£���20.0mL 0.20mol/LCH3COONa��Һ�еμ�0.20mol/L��ϡ���ᡣ��Һ��Phֵ�ı仯��ϵ����ͼ��ʾ��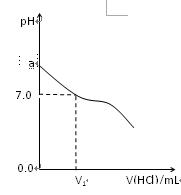
(1) a ��7.0�������ǣ������ӷ���ʽ��ʾ��?
��2����ͼ��������ϡ��������ΪV1mLʱ����Һ��pHֵ�պ�Ϊ7.0����ʱ��Һ��c(Cl-)?c(CH3COOH)�������������Ҫд���ж�����?
��3�����������������Ϊ20.0mLʱ���ⶨ��Һ�е�c(H+)Ϊ1.3��10-3 ?mol/L����CH3COH�ĵ���ƽ�ⳣ��Ka(������������λ��Ч����)��
�ο��𰸣���1��CH3COO- + H2O  ?CH3COOH + OH-?��3�֣�
?CH3COOH + OH-?��3�֣�
(2) ="?" ��2�֣� ���ݵ���غ��У�c(OH- ) + c(Cl- ) + c(C H3COO- ) = c(H+) + c(Na+) ������Һ��pH=7��c(OH- ) = c(H+)������c(Cl- ) + c(CH3COO- ) = c(Na+)��2�֣��������������غ��У�c(CH3COO H) + c(CH3COO- ) ="?" c(Na+)��1�֣�?������c(CH3COO H) = c(Cl- )��1�֣�
(3)�⣺��������������Ϊ20.0mLʱ���������ʸպ���ȫ��Ӧ������c(CH3COOH) =" 0.10mol/L?"
CH3COOH  ?CH3COO- + H+
?CH3COO- + H+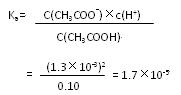
�����������
�����Ѷȣ���
2��ѡ���� ������ʵ��˵������ �����������(? )
�����������(? )
��1mol/LHCOOH��pH=2
�ڼ�������ˮ������Ȼ���
��20mL 1mol/LHCOOH��20mL 1mol/LNaOHǡ���к�
��HCOONa��Һ��pH>7
A���٢�
B���ڢ�
C���ۢ�
D���٢�
�ο��𰸣�
D
���������
������������ʣ�������ȫ���룬����1mol/LHCOOH��pH=2˵��HCOOH���ֵ��룬���Ԣٿ���֤��HCOOH�����ᡣ��˵���Ǽ�����ܽ�ȣ������ʵ�ǿ���ء���ֻ��˵��HCOOH��һԪ�ᣬ��ǿ���ء���HCOONa��Һ��pH>7��˵��HCOO��ˮ���Լ��ԣ����ݡ�˭��˭ˮ�⡱����֤��HCOOH�����ᡣ���Ԣ٢ܿ���֤��HCOOH�����ᣬD��ȷ��
�����Ѷȣ���
3������� ��4�֣�Ŀǰ�����ѿ��������õ���Դ�У�������������������Դ֮һ����֪��Ӧ��
2H2��O2 2H2O���Իش��������⣺
2H2O���Իش��������⣺
��1���÷�ӦΪ ��Ӧ������ȡ����ȡ�����
��2��������18g H2Oʱ��H2O�����ʵ����� ������ĸ���ţ���
A��1mol
B��1mol/L
C��1g/mol
D��18ml
�ο��𰸣����ȣ� A
�����������1��������������������Դ֮һ����÷�Ӧ�Ƿ��ȷ�Ӧ����2��������18g H2Oʱ��H2O�����ʵ�����18/18=1mol��ѡA��
���㣺���黯ѧ��Ӧ�е������仯��
�����Ѷȣ�һ��
4��ѡ���� �����и����У���ʹˮ�ĵ���ƽ�����������ƶ���������Һ��pHС��7��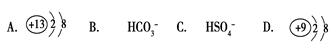
�ο��𰸣�A
���������
��ȷ��:A
A��Al3��ˮ������ԣ��ٽ�ˮ���룬pHС��7��A��ȷ��
B��ˮ�⣬�ٽ�ˮ���룬��pH����7��
C��ǿ����ʣ�����ˮ���룻
D��F�Dˮ�⣬�ٽ�ˮ���룬ˮ���pH����7.
�����Ѷȣ�һ��
5��ѡ���� �����Ȼ�ѧ����ʽ�С�H����ȼ���ȵ���
[? ]
A��CH4(g) + 3/2O2(g) = 2H2O(l) + CO(g) ��H1
B��S(s) + 3/2O2(g) = SO3(s) ��H2
C��C6H12O6(s) + 6O2(g) = 6CO2(g) + 6H2O(l)��H3
D��2CO(g) + O2(g) = 2CO2(g) ��H4
�ο��𰸣�C
���������
�����Ѷȣ���