ʱ��:2017-09-25 16:35:25
1��ѡ���� ����w1��w2�ֱ��ʾŨ��Ϊc1mol/L��c2mol/L�����������������֪2 w1��w2���������ƶ���ȷ���ǣ�������ܶȱȴ�ˮ�Ĵ�
A��2c1��c2
B��2c2��c1
C��c2��2c1
D��c1<c2<2c1
�ο��𰸣�C
��������������ʵ�����Ũ��Ϊc1 mol?L-1���ܶ�Ϊ��1�����ʵ�����Ũ��Ϊc2mol?L-1������Һ���ܶ�Ϊ��2����
c1= 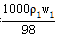 ��c2=
��c2= 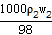 ��
��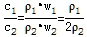 ����Ũ������ܶȴ���ˮ����Һ��Ũ��Խ���ܶ�Խ�����1����2��
����Ũ������ܶȴ���ˮ����Һ��Ũ��Խ���ܶ�Խ�����1����2��
��c2��2c1��
��ѡC��
���������⿼�����ʵ���Ũ�������������ļ�����Ƚϣ���Ŀ�Ѷ��еȣ�ע��Ũ������ܶȴ���ˮ����Һ��Ũ��Խ���ܶ�Խ��
�����Ѷȣ���
2��ѡ���� ��25��ˮ�м����������ʣ�����ʹˮ�ĵ���ƽ�ⷢ���ƶ����ǣ�
A��KI
B��Ũ��ˮ
C��������
D����ˮ
�ο��𰸣�A
���������A��KI����ǿ��ǿ���Σ�û�������ӣ���ˮ�⣬����ʹˮ�ĵ���ƽ�ⷢ���ƶ�
B Ũ��ˮ�����������ˮ�ĵ���
C�������������ᣬ������ˮ�ĵ���
D ���ȣ���ٽ�ˮ�ĵ��롣
��ѡA��
�����Ѷȣ�һ��
3��ѡ���� ����������ȷ���ǣ�?��
A��95�洿ˮ��pH<7��˵�����ȿɵ���ˮ������
B��pH=3�Ĵ�����Һ��ϡ����10����pH=4
C��0.2 mol?L-1�����ᣬ������ˮ��Ϻ�pH=1
D��pH=3�Ĵ�����Һ����pH=11������������Һ�������Ϻ�pH=7
�ο��𰸣�C
������������ȴٽ�ˮ�ĵ��룬����ˮ��Ȼ�����ԣ�A����ȷ�����������ᣬϡ�������ڵ��룬����ϡ����10����pH��4��B����ȷ��������ǿ�ᣬ����0.2 mol?L-1�����ᣬ������ˮ��Ϻ�Ũ����0.1mol/L������pH��1��C��ȷ��pH=3�Ĵ�����Һ��Ũ�ȴ���10��3mol/L�����Ժ��������Ʒ�Ӧ�����ǹ����ģ������Һ�����ԣ�D����ȷ�����Դ�ѡC��
�����Ѷȣ�һ��
4��ѡ���� ������0.1mol��L-1NaOH��Һ�ζ�a mLijŨ�ȵ�HCl��Һ���ﵽ�յ�ʱ����b mLNaOH��Һ����ʱ��Һ�������ӵ�Ũ��c(H+)/mol��L-1��(? )
A��0.1a/(a+b)
B��0.1b/(a+b)
C��1��107
D��1��10-7
�ο��𰸣�D
���������ǿ���ǿ��ǡ�÷�Ӧ�ǣ���Һ�����ԡ�����¶��dz��£���������Ũ����1��10-7mol/L����ѡD��
�����Ѷȣ�һ��
5��ѡ���� �ò����缫���500 mL��KNO3��Cu��NO3��2�Ļ����Һһ��ʱ���������������11��2L��״���µ����壬ԭ��Һ��Cu2+�����ʵ���Ũ��Ϊ��?��
A��0��5 mol��L
B��2 mol��L
C��l mol��L
D����ȷ��
�ο��𰸣�C
���������
��ȷ�𰸣�C
�ù�������������Ӧ���ȵ��Cu (NO3)2��Һ������ˮ
2H2O 2H2��?��? O2��
2H2��?��? O2��
0.5mol? 0.25mol
2Cu(NO3)2��2H2O 2Cu��O2����4HNO3
2Cu��O2����4HNO3
0.5mol? 0.5mol�D0.25mol
C(Cu2��)=0.5mol/0.5?L=l mol��L
�����Ѷȣ���