时间:2017-09-25 16:25:09
1、选择题 现有常温下pH=3的醋酸和pH=3的硫酸两种溶液,下列叙述正确的是( )
A.两溶液中水电离出的c(H+)均为1×10-11?mol?L-1
B.加水稀释100倍后两溶液的pH仍相同
C.醋酸中的c?(CH3COO-)?和硫酸中的c?(SO4 2- )相同]
D.等体积的两溶液中分别加入足量锌片时放出H2的体积相同
参考答案:A.pH=3的醋酸和pH=3的硫酸两种溶液中,存在离子积常数,[H+]酸?[OH-]水=10-14,所以两溶液中水电离出的c(H+)均为1×10-11mol?L-l,故A正确;
B.加水稀释100倍后两溶液的pH不相同,醋酸存在电离平衡,稀释pH增大程度小,而硫酸pH增大多,故B错误;
C.根据电荷守恒得C(H+)=C(CH3COO-)+C(OH-),C(H+)=2C(SO42-)+C(OH-),pH相对的醋酸和硫酸,氢离子浓度相等,则氢氧根离子浓度相等,所以醋酸根离子浓度是硫酸根离子浓度的2倍,故C错误;
D.等体积两溶液中分别加入足量镁粉后放出H2的体积不相同,醋酸放出氢气多,因为醋存在电离平衡,溶质浓度大于硫酸浓度,故D错误;
故选A.
本题解析:
本题难度:简单
2、填空题 (8分)在一定温度下,有a. 醋酸 b.硫酸 c.盐酸三种酸:
(1)当三种酸物质的量浓度相同时,三种溶液中水的电离程度由大到小的顺序是
用a、b、c表示,下同)
(2) 当c(H+)相同、体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为 .反应所需时间的长短关系是______________________.
(3)将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是______________________.
参考答案: (1) a>c>b( 2分) (2)a=b=c(2 分)b=c>a ( 2分)(3) a>b=c(2 分)
本题解析:(1)硫酸是二元强酸,盐酸是一元强酸,醋酸是一元弱酸。酸中氢离子浓度越大,对水的抑制程度越大。三种酸中氢离子浓度大小顺序是硫酸、盐酸和醋酸,所以三种溶液中水的电离程度由大到小的顺序是a>c>b。
(2)开始时,氢离子浓度相同,所以反应速率相同;由于醋酸是弱酸,存在电离平衡,在反应过程中,会继续电离出氢离子,所以醋酸的反应速率大,时间少,即反应所需时间的长短关系是b=c>a。
(3)弱酸在稀释过程中会继续电离出氢离子,所以c(H+)由大到小的顺序是a>b=c。
本题难度:困难
3、选择题 常温时,下列叙述正确的是
A.pH=9的NH4Cl与NH3・H2O混合溶液中c(Cl-)>c(NH4+)
B.pH=2.5的可乐中c(H+)是pH=3.5的柠檬水中c(H+)的1 0倍
C.AgCl在0.1 mol/L CaCl2溶液和0.l mol/L NaCl溶液中的溶解度相同
D.1 mL l mol l L Na2CO3溶液加水稀释至100 mL,pH和Kw均减小
参考答案:B
本题解析:A、pH=9的NH4Cl与NH3・H2O混合溶液中NH3・H2O的电离程度大于NH4Cl的水解程度,所以c(Cl-)<c(NH4+),错误;B、pH=2.5的可乐中c(H+)=1×10-2.5mol/L,pH=3.5的柠檬水中c(H+)=1×10-3.5mol/L,前者是后者的10倍,正确;C、0.1 mol/L CaCl2溶液和0.l mol/L NaCl溶液中的氯离子的浓度不同,导致AgCl的溶解度不同,错误;D、Kw是温度常数,温度不变,Kw不变,错误,答案选B。w的判断,同一物质在不同溶剂中的溶解度的判断
本题难度:一般
4、选择题 已知液氨的性质与水相似,25℃时,NH3+NH3 NH4++NH2-,NH4+离子的平衡浓度为1×10-15mol/L,则下列说法中正确的是 ( )
NH4++NH2-,NH4+离子的平衡浓度为1×10-15mol/L,则下列说法中正确的是 ( )
A.在液氨中加入NaNH2可使液氨的离子积变大
B.在液氨中加入NH4Cl可使液氨的离子积减小
C.在此温度下液氨的离子积为1×10-30
D.在液氨中放入金属钠,可生成NaNH2
参考答案:CD
本题解析:略
本题难度:简单
5、选择题 有两种一元弱酸的钠盐溶液,其物质的量浓度相等,现向这两种盐的溶液中分别通入适量的CO2,发生如下反应:NaR+CO2+H2O=HR+NaHCO3 2NaR1+CO2+H2O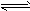 2HR1+Na2CO3;HR和HR1的酸性强弱比较,正确的是
2HR1+Na2CO3;HR和HR1的酸性强弱比较,正确的是
[? ]
A.HR较弱
B.HR1较弱
C.两者相同
D.无法比较
参考答案:B
本题解析:
本题难度:一般