时间:2017-09-24 00:20:57
1、实验题 Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
[实验设计]控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验。
(1)完成以下实验设计表(表中不要留空格)。

[数据处理]实验测得p―CP的浓度随时间变化的关系如图,①②③分别代表以上三组实验测得的数据曲线。
(2)请根据实验①曲线,计算降解反应在 50~150s内的平均反应速率;v(p―CP)=?
_________?mol L-1
L-1 s-1。
s-1。
(3)实验①、②表明温度升高,该降解反应速率_____。?(增大或减小)但其他文献表明,温度过高时(如接近100℃)反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:?_________________________________。
(4)实验③得出的结论是:pH等于10时,_________________________
(5)实验时需在不同时间从反应器中取样,并使所取样品中反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法:_____________________________。
2、实验题 (16分)为测定碳酸钙纯度(设含杂质SiO2),学生设计了如下几个实验方案。请回答每个方案中提出的问题。
【方案I】
(1)称取碳酸钙样品M g;
(2)加入过量盐酸;
(3)收集并测定生成的气体体积V mL。
问题1:反应结束后,量气管中的显示如右图所示,接下来的操作是:?,读出甲管中液面的读数。
【方案II】
(1)称取碳酸钙样品M g;
(2)用c mol/L 盐酸V mL(过量)溶解样品;
(3)取溶解后的溶液 mL,以酚酞作指示剂,用c′ mol/L NaOH溶液滴定,恰好用去V′mL。
mL,以酚酞作指示剂,用c′ mol/L NaOH溶液滴定,恰好用去V′mL。
问题2:列出本实验中所用到的主要仪器名称(除铁架台及附件、烧杯之外)?。
问题3:碳酸钙纯度计算公式?。
问题4:当碳酸钙溶解完全后,少量未溶的SiO2没过滤去,结果得到碳酸钙纯度________?(偏大、偏小或无影响)
【方案Ⅲ】
(1)称取碳酸钙样品M g;
(2)加入足量c mol/L盐酸V mL使之完全溶解;
(3)过滤并取滤液;
(4)在滤液中加入过量c′ mol/L Na2CO3溶液V′mL;
(5)将步骤(4)中的沉淀滤出、洗涤、干燥、称重为M′g。
问题5:此方案中不需要的数据是?(填选项编号)。
A.c、V
B.c′、 V′
C. M′
D. M
问题6:为减少实验误差,步骤(3)、(5)过滤后都要对沉淀进行洗涤,如果步骤(3)未经洗涤,则测定的碳酸钙的纯度将?(偏大、偏小、无影响,下同);如果步骤(5)未经洗涤,则测定的碳酸钙纯度将?。
问题7:判断步骤(4)中Na2CO3溶液是否过量的方法是??。
3、实验题 某化学学习小组利用如图所示装置来探究相应物质的化学性质。选择适当试剂完成实验A、B、C,并得出相应的实验结论。实验A、B、C所用试剂和所得结论列于表中。?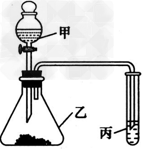
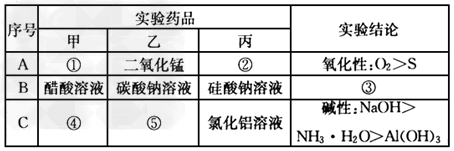
(1)乙装置的名称:_____________。 ?
(2)请填写①~⑤的试剂名称或实验结论:①___________;②__________;③________ ?;④___________;⑤______________。 ?
(3)小明利用该装置自行设计了一个实验――证明NO2具有氧化性(注:丙中已事先添加Na2S溶液)。据此回答下列问题: ?
①如何检验该装置的气密性:_______; ?
②打开甲装置的活塞后,装置乙中发生反应的化学方程式:___________; ?
③某同学对小明的实验设计提出了质疑,认为丙中溶液变浑浊不足以证明NO2具有氧化性,你认为他的理由是:__________ (用化学反应方程式和简要文字回答); ?
④NO2气体有毒,应用NaOH溶液吸收,请写出此反应的离子方程式:____________。
4、实验题 (14分)油条是一种深受群众喜爱的传统食品,在百姓早餐桌上一直占有重要位置。但油条中铝含量超标问题十分普遍,是影响群众健康的食品安全隐患。从2009年5月下旬开始,浙江省的油条加工停用含铝食品的添加剂,逐步转换为无铝添加剂配方和工艺,从而保证百姓吃上安全、放心的油条。油条无铝配方由碳酸氢钠(小苏打)、碳酸氢铵(臭粉)组成。为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如下装置进行实验。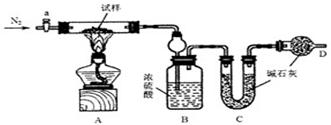

实验过程
①按图组装仪器,检查装置的气密性;
②将试样m1g放入硬质玻璃管中,装置B、C、D中药品如图,已知加药品后装置B的质量为m2g、装置C的质量为m3g;
③关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;
④称得装置B的质量为m4g、装置C的质量为m5g。
请回答以下问题(装置中原有空气对实验的影响忽略不计 ):
):
(1)装置A中发生反应的化学方程式为?▲?。
(2)装置B的作用为?▲?。
装置C的作用为?▲?。
(3)实验过程中通入N2的目的为?▲?。
(4)用下列各项所提供的数据能计算出w(NaHCO3)的是(?▲?)(填选项字母)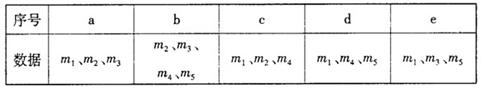
(5)实验结束后发现装置A中硬质玻璃管右端有水珠,你认为利用实验中所提供的数据还能否得到准确的w(NaHCO3)?▲?(填“能”或“不能”)。若能,则w(NaHCO3)的计算式为:?▲?,若不能,此问不作答。
5、实验题 某研究性学习小组将一定浓度的Na2CO3溶液滴入CuSO4。溶液中得到蓝色沉淀。关于沉淀的成分,有以下几种假设:
假设1:沉淀是CuCO3;
假设2:沉淀是Cu(OH)2;
假设3:沉淀是_____________________________________。
(1)若假设1成立,则发生反应的离子方程式为_______________________________。
(2)若假设2成立,原因是__________________________________________________。
(3)该研究性学习小组拟用以下装置测定沉淀成分,请完成下表。已知:①CuCO3和Cu(OH)2均不带结晶水;②装置气密性良好;③原装置中的空气对实验结果的影响可忽略。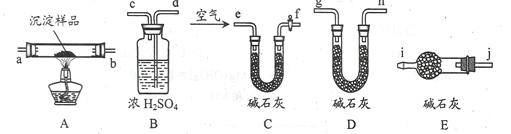
| 实验步骤 | 预期现象 | 结论 |
| ①称量B、D的质量分别为ml、m2,将装置按? f→a→b→___→___→___→___→j→i顺序连接。? | ? | ? |
| ②称取一定质量的沉淀______________________,然后___________________,冷却后再称量B、D的质量分别为m3、 m4 | (1)若m1 = m3,m2 < m4 (2)若m1___m3,m2___m4 (3)若ml___m3,m2___m4 | (1)假设1成立 (2)假设2成立 (3)假设3成立 |