时间:2017-09-23 23:19:16
1、实验题 某课外活动小组拟用下列装置做炼铁原理的实验,同时检测氧化铁的纯度(假设矿石不含其他与CO 反应的成分),并除去尾气。CO用反应H2C2O4 = CO2↑+CO↑+H2O来制取。与Fe2O3反应的CO需纯净、干燥。 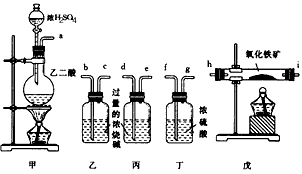
(1)若所制的气体的流向为从左向右时,下列仪器组装连接的顺序是(用a"b……表示)____接 ____,___接____,____接 ____,____接___。
(2)装置乙的作用是________________。
(3)实验结束后,先熄灭戊处的酒精灯,再熄灭甲处的酒精灯,其主要原因是_______________。
(4)实验前氧化铁矿粉末的质量为xg,实验后测得乙和丙的质量分别增加了yg和zg,则氧化铁矿粉末中氧化铁的质量分数为____。
参考答案:(1)a;b;c;f;g;h;l;d或a;d;e;f;g;h;i;b
(2)吸收CO2
(3)防止还原产生的Fe受热时被氧化
(4)40y/33x×100%或40z/33x×100%
本题解析:
本题难度:一般
2、实验题 某实验小组用下列装置进行乙醇催化氧化的实验。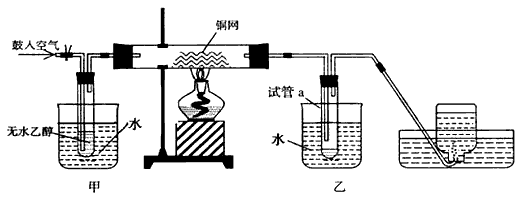
⑴实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式_____________________、
_____________________。在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该反应是
_____反应(填“吸热” 或“放热”)。
⑵甲和乙两个水浴作用不相同。甲的作用是____________;乙的作用是____________。
⑶反应进行一段时间后,于试管a中能收集到不同的物质,它们是乙醇、乙醛和____________,(填一种物质名称即可)。集气瓶中收集到的气体的主要成分是____________(填物质名称或化学式)。
⑷若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有____________(填物质名称或化学式)。要除去该物质,可现在混合液中加入____________(填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化
碳然后,还要通过____________(填试验操作名称)才能得到较纯的乙醛。
参考答案:⑴ 2Cu+O2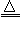 2CuO;CH3CH2OH+CuO
2CuO;CH3CH2OH+CuO CH3CHO+Cu+H2O;放热
CH3CHO+Cu+H2O;放热
⑵加热;冷凝
⑶水;氮气
⑷乙酸;c;蒸馏
本题解析:
本题难度:一般
3、选择题 从下列事实所得出的相应结论正确的是(? )
| 序号 | 实验事实 | 结论 |
| ① | Cl2的水溶液可以导电 | Cl2是电解质 |
| ② | 将燃烧的镁条放入CO2中能继续燃烧 | 还原性:Mg>C |
| ③ | 常温下白磷可自燃而氮气须在放电时才与氧气反应 | 非金属性:P>N |
| ④ | 某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中一定有NH4+ |
参考答案:B
本题解析:氯水导电是因为氯气与水反应的产物盐酸及次氯酸是电解质,氯气不是电解质,①错;镁与CO2的反应中镁是还原剂,C是还原产物,②正确;P在常温下即与氧气反应,而N2要在放电情况下才能与氧气反应,是因为N2分子中的叁键键能特别大使得反应的活化能很大,而且元素的非金属性取决于其得电子能力,在上述两个反应中N和P均表现为还原性而非氧化性,③错;中学范围内能使湿润的红色石蕊试纸变蓝色的气体一定是氨气,而某溶液能与氢氧化钠溶液共热产生氨气则可说明溶液中含有铵根离子,④正确。
本题难度:一般
4、实验题 经测定乙醇的化学式是C2H6O,由于有机物普遍存在同分异构现象,推测乙醇的结构可能是下列两种之一。 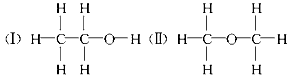
为测定其结构,应利用物质的特殊性进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,请甲、乙、丙、丁四位同学直接利用如图给定装置开始进行实验确定乙醇的结构。 
(1)学生甲得到一组实验数据如下表:根据以上数据推断乙醇的结构为_______(用Ⅰ、Ⅱ表示),理由为_____________________ ; 
(2)同学乙分别准确称量4.60 g 乙醇进行多次实验,结果发现以排在量筒内水的体积作为生成的H2体积,换算成标准状况后都小于1.12L,如果忽略量筒本身及乙同学读数造成的误差,那么乙认为可能是由于样品中含有少量水造成的,你认为正确吗?_________ (填“正确”或“不正确”)。如果你认为正确,请说明理由;如果你认为不正确,那产生这种情况的原因应该是什么?____________________
(3)同学丙认为实验成功的关键有:①装置气密性要良好,②实验开始前准确确定乙醇的量,③钠足量,④广口瓶内水必须充满,⑤氢气体积的测算方法正确、数据准确。
其中正确的有________________ 。(填序号)
(4)同学丁不想通过称量乙醇的质量来确定乙醇的量,那么还需要知道的数据是________________
(5)实验后,四名同学从乙醇的可能结构分析入手,对乙醇和钠的量的关系进行了讨论,如果乙醇的物质的量为n mol,那么对钠的物质的量的取值要求必须是____________________ 。
参考答案:(1)I;因为n(Na)/n(H2)=0.10/0.05=2∶1,所以1个钠能置换乙醇中的1个H原子
(2)不正确;因为混有水产生的氢气大于1.12L,可能乙醇中混有丙醇等杂质,或者加入的钠不够。
(3)① ② ③ ⑤?
(4)乙醇的密度和体积
(5)大于n
本题解析:
本题难度:一般
5、实验题 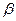 ―锂辉石的主要成分是Li2O・Al2O3・4SiO2,还含有FeO、CaO、MgO等。
―锂辉石的主要成分是Li2O・Al2O3・4SiO2,还含有FeO、CaO、MgO等。
以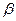 ―锂辉石为原料制备碳酸锂的一种流程如下:
―锂辉石为原料制备碳酸锂的一种流程如下: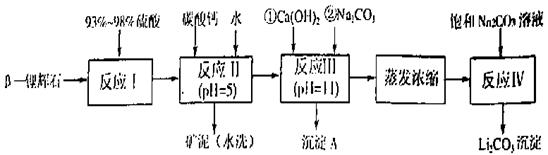
已知:①部分金属氢氧化物开始沉淀和完全沉淀的pH:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.7 | 9.6 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
| 温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
参考答案:
(1)除去反应Ⅰ中过量的硫酸,控制pH使Fe 3+、Al3+完全沉淀(3分)
(2)Mg2++2OH-= Mg(OH)2↓(2分)? Ca2++CO32-=CaCO3↓(2分)
(3)Li2SO4+Na2CO3=Li2CO3↓+Na2SO4(3分)
碳酸锂在较高温度下溶解度小,用热水洗涤可减少碳酸锂的损耗(3分)
(4)ABD(3分)
本题解析:略
本题难度:简单