时间:2017-08-26 01:31:15
1、选择题 下列常用实验室仪器中,一般不用于混合物分离或提纯的是
A.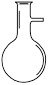
B.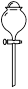
C.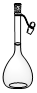
D.
参考答案:C
本题解析:一般用于混合物分离或提纯的操作是过滤、蒸馏、萃取或分液,常用的仪器分别是漏斗、蒸馏烧瓶、分液漏斗。根据装置特点可知,A~D分别是蒸馏烧瓶、分液漏斗、容量瓶和漏斗。容量瓶常用来配制一定物质的量浓度,不用于物质的分离和提纯,因此正确的答案选C。
本题难度:简单
2、选择题 下列几种情况,对中和滴定结果无影响的是
A.滴定管用水冲洗后即注入标准液
B.锥形瓶里有少量水
C.滴定前标准液在“0”刻度以上
D.滴定管尖端未充满液体
参考答案:B
本题解析:根据c(待)=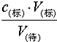 判断不当操作对相关物理量的影响。A、滴定管用水冲洗后即注入标准液,则标准液浓度降低,造成V(标)偏大,根据c(待)=
判断不当操作对相关物理量的影响。A、滴定管用水冲洗后即注入标准液,则标准液浓度降低,造成V(标)偏大,根据c(待)=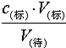 可知测定结果偏高,A不正确;B、盛待测液的锥形瓶里留有蒸馏水,对V(标)无影响,根据c(待)=
可知测定结果偏高,A不正确;B、盛待测液的锥形瓶里留有蒸馏水,对V(标)无影响,根据c(待)=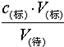 可知,c(待)不变,故B正确;C、滴定前标准液在“0”刻度以上,则造成V(标)偏小,根据c(待)=
可知,c(待)不变,故B正确;C、滴定前标准液在“0”刻度以上,则造成V(标)偏小,根据c(待)=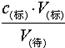 可知,c(待)偏小,C不正确;D、滴定管尖端未充满液体,造成V(标)偏大,根据c(待)=
可知,c(待)偏小,C不正确;D、滴定管尖端未充满液体,造成V(标)偏大,根据c(待)=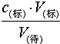 可知,c(待)偏大,D不正确,答案选B。
可知,c(待)偏大,D不正确,答案选B。
本题难度:一般
3、选择题 根据下图所示的装置进行相关实验,对实验现象预测正确的是(?)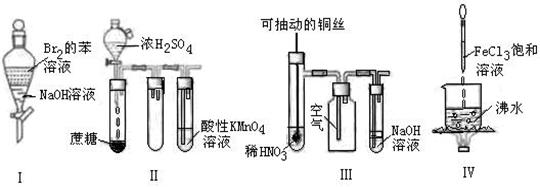
A.实验I:振荡后静置,上层溶液颜色保持不变
B.实验II:酸性KMnO4溶液中出现气泡,且颜色不会褪去
C.实验III:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色
D.实验IV:溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应
参考答案:D
本题解析:单质溴能和氢氧化钠反应,所以溶液褪色,A不正确。浓硫酸具有脱水性和强氧化性,在反应中能产生SO2,SO2具有还原性,能使酸性高锰酸钾溶液褪色,B不正确。铜和稀硝酸反应生成NO。NO极易被氧化生成红棕色NO2气体,C不正确,所以正确的答案选D。
本题难度:一般
4、选择题 下列实验操作,处理方法错误的是
A.做银镜反应的试管先用NaOH溶液洗涤,倒掉后再用清水冲洗干净
B.皮肤上若沾有少量的苯酚用酒精洗
C.做银镜反应后的试管一般采用浓盐酸洗涤
D.制乙烯的实验温度计应伸入液面下
参考答案:C
本题解析:银镜反应中产生的银不能溶解在浓盐酸液中,应该用硝酸洗涤,C不正确,其余选项都是正确的,答案选C。
点评:该题是基础性试题的考查,主要是考查学生对有机化学实验基本操作的了解掌握程度,有利于培养学生的综合实验能力,提高学生的规范实验设计和操作能力。
本题难度:一般
5、选择题 用NA表示阿伏加德罗常数的数值,下列说法中正确的是
A.盛有CO2的密闭容器中含有NA个氧原子,则C的物质的量不一定是0.5mol
B.常温下,5.6g铁与足量的盐酸反应,失去的电子数为0.3NA
C.常温常压下,氧气和臭氧的混合物16g中含有NA个氧原子
D.1mol?L-1NaCl溶液含有NA个Na+离子
参考答案:C
本题解析:分析:A、根据n=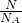 计算氧原子的物质的量,结合二氧化碳的分子式计算碳原子的物质的量.
计算氧原子的物质的量,结合二氧化碳的分子式计算碳原子的物质的量.
B、铁与盐酸反应生成氯化亚铁,铁表现+2价,据此计算转移电子数.
C、氧气和臭氧都是由氧元素组成的,16g为氧原子的质量,根据n=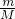 计算氧原子的物质的量,再根据N=NA计算氧原子数目.
计算氧原子的物质的量,再根据N=NA计算氧原子数目.
D、溶液体积未给出,无法计算.
解答:A、氧原子的物质的量为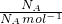 =1mol,氧原子与碳原子的物质的量之比为2:1,所以碳原子的物质的量为1mol×
=1mol,氧原子与碳原子的物质的量之比为2:1,所以碳原子的物质的量为1mol× =0.5mol,故A错误;
=0.5mol,故A错误;
B、铁与盐酸反应生成氯化亚铁,铁表现+2价,5.6g铁与足量的盐酸反应失去的电子数为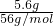 ×2×NAmol-1=0.2NA,故B错误;
×2×NAmol-1=0.2NA,故B错误;
C、氧气和臭氧都是由氧元素组成的,16g为氧原子的质量,所以16g氧气和臭氧的混合物中含氧原子数为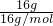 ×NAmol-1=NA,故C正确;
×NAmol-1=NA,故C正确;
D、溶液体积未给出,无法计算钠离子数目,故D错误.
故选:C.
点评:考查常用化学计量数的有关计算,难度不大,注意铁与盐酸反应生成氯化亚铁,与氯气反应生成氯化铁.
本题难度:一般