时间:2017-08-10 01:17:31
1、填空题 (8分)(每空2分)CH3COOH是中学化学中常用的一元弱酸,请回答下列问题:
(1)若分别将pH=2的盐酸和醋酸稀释100倍,则稀释后溶液的pH:盐酸 醋酸(填“>”、“=”或“<”)。
(2)将100mL 0.1mol・L-1的CH3COOH溶液与50mL 0.2mol・L-1的NaOH溶液混合,所得溶液呈 性,原因 (用离子方程式表示)。
(3)已知某混合溶液中只含有CH3COO-、H+、Na+、OH-四种离子,且离子浓度大小关系为:c(CH3COO-)> c(H+)> c(Na+)> c(OH-),则该溶液中含有的溶质为 。
(4)已知Ka(CH3COOH)= 1.76×10-5,Ka(HNO2)= 4.6×10-4,若用同浓度的NaOH溶液分别中和等体积且pH相等的CH3COOH和HNO2,则消耗NaOH溶液的体积关系为:前者 后者(填“>,<或=”)
参考答案:(1)> (2)碱 CH3COO-+H2O CH3COOH+OH-(3)CH3COOH和CH3COONa (4) >
CH3COOH+OH-(3)CH3COOH和CH3COONa (4) >
本题解析:(1)醋酸是弱酸,在加水稀释100倍时,醋酸继续电离,溶液的PH小于4,而盐酸是强酸,稀释100倍后,溶液的PH=4,所以稀释后溶液的PH:盐酸大于醋酸;
(2)醋酸和NaOH的物质的量相等,恰好反应生成强碱弱酸盐,溶液呈碱性,原因为CH3COO-水解打破了水的电离平衡所致,离子方程式为:CH3COO-+H2O CH3COOH+OH-;
CH3COOH+OH-;
(3)某混合溶液中只含有CH3COO-、H+、Na+、OH-四种离子,且离子浓度大小关系为:c(CH3COO-)> c(H+)> c(Na+)> c(OH-),说明溶液呈酸性,且溶液的电离程度大于水解程度,所以溶质有CH3COOH和CH3COONa;
(4)根据Ka的大小可知,,Ka(HNO2)> Ka(CH3COOH),根据电离平衡常数越大,酸性越强,所以HNO2酸性大于醋酸,pH相等的CH3COOH和HNO2,醋酸的浓度大于亚硝酸,若用同浓度的NaOH溶液分别中和等体积且pH相等的CH3COOH和HNO2,则消耗NaOH溶液的体积关系为:醋酸大于亚硝酸。
考点:考查PH的大小比较,溶液的酸碱性,离子浓度的大小比较等知识。
本题难度:困难
2、选择题 已知弱酸的电离平衡常数如下表: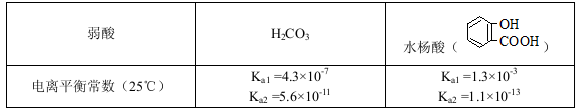
下列选项正确的是
A.常温下,等浓度、等体积的NaHCO3溶液pH小于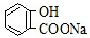 溶液pH
溶液pH
B.常温下,等浓度、等体积的Na2 CO3溶液和 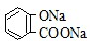 溶液中所含离子总数前者小于后者
溶液中所含离子总数前者小于后者
C.
D.水杨酸的第二级电离 Ka2远小于第一级电离Ka1的原因之一是 能形成分子内氢键
参考答案:D
本题解析:根据碳酸、水杨酸电离平衡常数的数据,常温下,等浓度、等体积的NaHCO3溶液pH大于溶液pH,A不正确;常温下,等浓度、等体积的Na2CO3溶液pH小于和溶液pH,根据溶液中电荷守恒,Na2CO3溶液和溶液中所含离子总数前者大于后者,B不正确;NaHCO3只与-COOH反应,C不正确;根据结构能形成分子内氢键,D正确
考点:化学基本理论
本题难度:一般
3、选择题 常温时,将CH3COOH溶液和NaOH溶液等体积混合后,溶液呈中性。则下列各项正确的是? ( )。
A.混合前:pH(CH3COOH)+pH(NaOH)=14
B.混合后:c(Na+)=c(CH3COO-)+c(OH-)
C.混合前:c(CH3COOH)>c(NaOH)
D.混合后:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
参考答案:C
本题解析:混合前,若pH(CH3COOH)+pH(NaOH)=14,则,c(H+)=c(OH-),CH3COOH为弱电解质,部分电离,c(CH3COOH)比c(NaOH)大得多,混合后不会呈中性而是呈酸性,故A不正确,C正确;混合后溶液呈中性,则c(H+)=c(OH-),根据电荷守恒,c(Na+)=c(CH3COO-),故B、D不正确。
本题难度:一般
4、选择题 常温时,pH=2.7的一元弱酸溶液加水稀释,若溶液体积扩大10倍,则溶液中的变化是
[? ]
A. [H+]增大
B. [H+]、[OH-]都减小
C. [OH-]增大
D. [H+]×[OH-]不变
参考答案:CD
本题解析:
本题难度:简单
5、选择题 下列图示与对应的叙述相符的是  
  
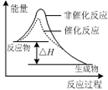

图甲 图乙 图丙 图丁
A.由图甲表示的反应速率随温度变化的关系可知该反应的ΔH>0
B.图乙表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是醋酸
C.图丙表示该反应为放热反应,且催化剂能改变反应的焓变
D.图丁表示向Na2CO3溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸物质的量的关系
参考答案:B
本题解析:A、图像中交叉点左边是未平衡时曲线,右边是平衡曲线,温度高,正反应速率小于逆反应速率,平衡逆向移动,反应放热,错误;B、醋酸是弱酸,稀释时电离程度增大,pH变化小,正确;C、催化剂只改变反应速率,不改变焓变,错误;D、逐滴加盐酸,首先生成碳酸氢钠然后才产生二氧化碳气体,错误。
考点:考查化学图像与原理有关问题。
本题难度:一般